题目内容
已知元素M是组成物质NH4Al(SO4)2的一种元素.元素M的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号I1至I4表示)如表所示:| I1 | I2 | I3 | I4 | 电离能(kJ/mol) | 578 | 1817 | 2745 | 11578 |
分析:从其电离能变化知,当原子失去第四个电子时,其电离能急剧增加,说明该元素失去三个电子时为稳定结构,则该元素最外层有3个电子,据此分析解答.
解答:解:从其电离能变化知,当原子失去第四个电子时,其电离能急剧增加,说明该元素失去三个电子时为稳定结构,则该元素最外层有3个电子,N原子最外层有5个电子、Al氧原子最外层有3个电子、Si原子最外层有4个电子、S原子最外层有6个电子、O原子最外层有6个电子,所以符合条件的是Al元素,故答案为:铝.
点评:本题考查了元素电离能与原子最外层电子数之间的关系,当电离能急剧增大时,说明该离子由稳定结构变化而来,据此判断该原子最外层电子数,难度不大.

练习册系列答案
相关题目
已知元素M是组成物质NH4Al(SO4)2的一种元素。元素M的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号I1至I4表示)如下表所示:
|
|
I1 |
I2 |
I3 |
I4 |
|
电离能(kJ/mol) |
578 |
1817 |
2745 |
11578 |
(1)元素M的名称是_______________;
(2)硫原子核外有______种不同运动状态的电子,有______种不同形状的电子云;
(3)请用一个事实证明氧气的氧化性比硫的氧化性强:______________________________。
(4)相同条件下,0.1 mol/L NH4Al(SO4)2中c(NH4+)________(填“等于”、“大于”或“小于”)0.1 mol/LNH4HSO4中c(NH4+)。
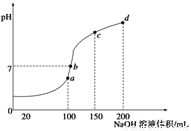
(5)室温时,向100 mL 0.1 mol/LNH4HSO4溶液中滴加0.1 mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
①试分析图中a、b、c、d四个点,水的电离程度最大的是____________;
②在b点,溶液中各离子浓度由大到小的排列顺序是________;
③在c d段发生反应的离子方程式_________________。
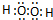
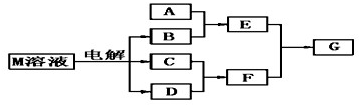
 (4)若A是一种常见的化肥,式量为79,且E与F生成G时有白烟产生,则A的化学式
(4)若A是一种常见的化肥,式量为79,且E与F生成G时有白烟产生,则A的化学式