题目内容
某混合气体的质量分数:H2为72%,N2为28%,计算该混合气体的平均相对分子质量。
解析:先假设混合气体的总质量为m(总),根据混合气体的质量分数,求出各组分的物质的量,进而求出n(总),再根据![]() =
=![]() 求出平均摩尔质量,也就是平均相对分子质量。
求出平均摩尔质量,也就是平均相对分子质量。
设此混合气体的总质量为m(总),则:
n(H2)=![]() =
=![]()
n(N2)=![]() =
=![]()
所以:n(总)=n(H2)+n(N2)
![]() =
=![]() =
= =
= g·mol-1=2.70 g·mol-1
g·mol-1=2.70 g·mol-1
答案:此混合气体的平均相对分子质量为2.70。

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
某混合气体中各气体的质量分数为N2 14%,CO2 22%,CH4 64%,则此混合气体对氢气的相对密度为
| A.10 | B.14.2 | C.20 | D.32 |
 32%,
32%, 28%,
28%, 22%,
22%, 16%,
16%, 2%,此混合气体对
2%,此混合气体对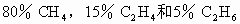 ,计算0.500mol该混合气体的质量和标准状况下的密度(g/L).
,计算0.500mol该混合气体的质量和标准状况下的密度(g/L).
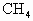 在一定条件下催化氧化可以生成
在一定条件下催化氧化可以生成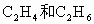 (水和其它反应产物忽略不计).取一定量
(水和其它反应产物忽略不计).取一定量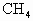 经催化氧化后得到一种混合气,它在标准状况下的密度为0.780g/L.已知反应中
经催化氧化后得到一种混合气,它在标准状况下的密度为0.780g/L.已知反应中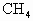 消耗了20.0%,计算混合气体中
消耗了20.0%,计算混合气体中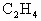 的体积分数.(计算结果保留3位有效数字)
的体积分数.(计算结果保留3位有效数字)