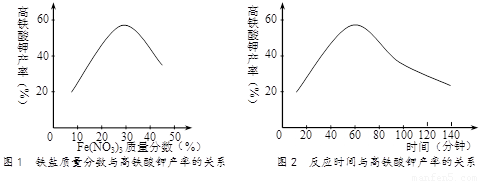题目内容
KClO3在农业上用作除草剂,超细CaCO3广泛用于消光纸、无炭复写纸等.某同学在实验室模拟工业过程,利用制乙炔产生的残渣制备上述两种物质,过程如下:
Ⅰ.![]()
①电石与水反应的化学方程式是________.
②残渣中主要成分是Ca(OH)2和________.
Ⅱ.将Ⅰ中的部分灰浆配成浊液,通入Cl2,得到Ca(ClO3)2与CaCl2物质的量之比为1∶5的溶液,反应的化学方程式是________.
Ⅲ.向Ⅱ所得溶液中加入KCl,发生复分解反应,经蒸发浓缩,冷却结晶,过滤得KClO3晶体.你认为能得到KClO3晶体的原因是________________.
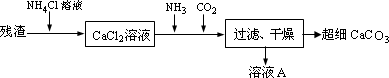
Ⅳ.将Ⅰ中的残渣溶于NH4Cl溶液,加热,收集挥发出的气体再利用.向所得CaCl2溶液中依次通入NH3、CO2,便可获得超细CaCO3,过程如下:
①根据沉淀溶解平衡原理,解释残渣中难溶盐的溶解原因________________.
②CaCl2溶液中通入两种气体后,生成超细CaCO3的化学方程式是________.
③图示的溶液A可循环使用,其主要成分的化学式是________.
答案:
解析:
解析:
|
Ⅰ.①CaC2+2H2O Ⅱ.6Cl2+6Ca(OH)2 Ⅲ.KClO3的溶解度小 Ⅳ.①CaCO3(s) ②CaCl2+2NH3+CO2+H2O ③NH4Cl |

练习册系列答案
相关题目
 Ca(OH)2+C2H2↑ ②CaCO3
Ca(OH)2+C2H2↑ ②CaCO3 5CaCl2+Ca(ClO3)2+6H2O
5CaCl2+Ca(ClO3)2+6H2O CaCO3↓+2NH4Cl
CaCO3↓+2NH4Cl


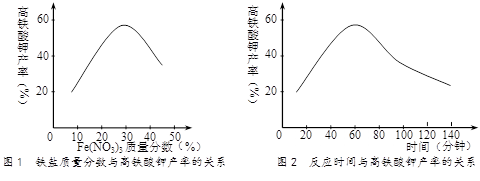

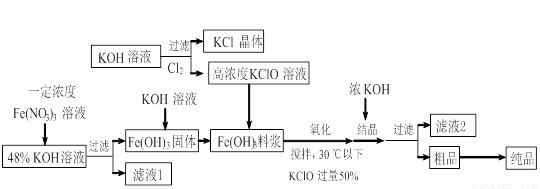
 ,工业上用湿法制备高铁酸钾的基本流程如下图所示:
,工业上用湿法制备高铁酸钾的基本流程如下图所示:
 。
。

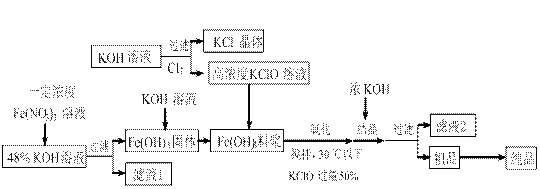
 ▲ 。
▲ 。 O3的混合溶液,经测定ClO-与ClO3-离子的物质的量之比是1:2,则Cl2与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为 ▲ 。
O3的混合溶液,经测定ClO-与ClO3-离子的物质的量之比是1:2,则Cl2与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为 ▲ 。