题目内容
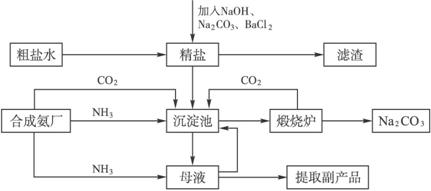
我国化学家侯德榜(右下图),改革国外的纯碱生产工艺,生产流程可简要表示如下:

(1)上述生产纯碱的方法称___________,副产品的一种用途为______________________。
(2)沉淀池中发生的化学反应方程式是_______________________________________。
(3)写出上述流程中X物质的分子式___________。
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了___________(填上述流程中的编号)的循环,从沉淀池中取出沉淀的操作是___________。
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加_______________。
(6)向母液中通氨气,加入细小食盐颗粒,冷却析出副产品。通氨气的作用有___________。
a.增大![]() 的浓度,使NH4Cl更多地析出
的浓度,使NH4Cl更多地析出
b.使NaHCO3更多地析出
c.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
解析:本题主要是考查侯德榜制碱法的生产原理及生产工艺,Cl-的检验等,根据联合制碱法的生产原理,可知向食盐水中通入氨气是为了得到碱性溶液,以吸收更多的CO2,当CO2过多时发生反应会发生一系列的反应。产生碳酸氢钠沉淀,此沉淀受热会分解产生二氧化碳气体。要提高氯化钠的利用率必须将过滤后的碳酸氢钠的母液循环利用。要检验碳酸钠中是否混有氯化钠,只需向其溶液中加入硝酸酸化的硝酸银溶液,看是否有白色沉淀生成。
答案:(1)联合制碱法或侯德榜制碱法 作化肥或电解液或焊药等(其他合理答案均可)
(2)NH3+CO2+H2O+NaCl![]() NH4Cl+NaHCO3↓或NH3+CO2+H2O
NH4Cl+NaHCO3↓或NH3+CO2+H2O![]() NH4HCO3
NH4HCO3
NH4HCO3+NaCl![]() NaHCO3↓+NH4Cl
NaHCO3↓+NH4Cl
(3)CO2
(4)Ⅰ 过滤
(5)稀HNO3或AgNO3溶液
(6)ac

 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案

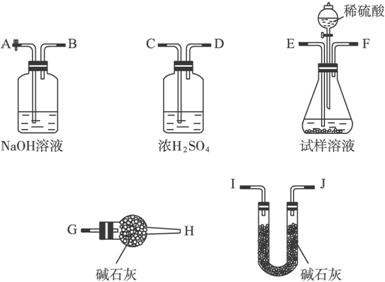
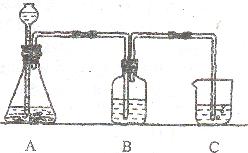 ①配制含氨的氯化钠饱和溶液;②用石灰石和稀盐酸制取纯净的CO2;③将CO2通入NaCl的氨溶液中,得到碳酸氢钠晶体:④过滤,冷水洗涤沉淀;⑤焙烧NaHCO3得到Na2CO3。
①配制含氨的氯化钠饱和溶液;②用石灰石和稀盐酸制取纯净的CO2;③将CO2通入NaCl的氨溶液中,得到碳酸氢钠晶体:④过滤,冷水洗涤沉淀;⑤焙烧NaHCO3得到Na2CO3。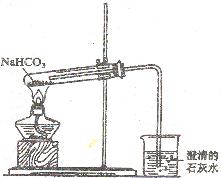 试管中发生的化学反应方程式是:
试管中发生的化学反应方程式是: