题目内容
(14分)我国化学家侯德榜根据NaHCO3的溶解度比NaCl、Na2CO3、NH4C1都小的性质,运用![]() 等反应原理,发明了“侯氏制碱法”。
等反应原理,发明了“侯氏制碱法”。
根据侯德榜制碱法原理,实验室用食盐、氨水、犬理石、盐酸制取碳酸钠。其实验过程如下:
 ①配制含氨的氯化钠饱和溶液;②用石灰石和稀盐酸制取纯净的CO2;③将CO2通入NaCl的氨溶液中,得到碳酸氢钠晶体:④过滤,冷水洗涤沉淀;⑤焙烧NaHCO3得到Na2CO3。
①配制含氨的氯化钠饱和溶液;②用石灰石和稀盐酸制取纯净的CO2;③将CO2通入NaCl的氨溶液中,得到碳酸氢钠晶体:④过滤,冷水洗涤沉淀;⑤焙烧NaHCO3得到Na2CO3。
试回答下列问题:
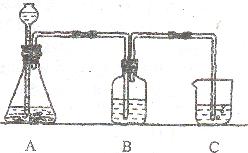
(1)某学生将实验步骤④、③、③设计成下图所示的装置:洗气瓶B中的液体是 ,烧杯C中的液体是 。
(2)实验步骤④中洗涤沉淀的目的是 。
(3)该学生设计右图所示装置进行NaHCO3的分解,并证实产物中有C02产生。
① 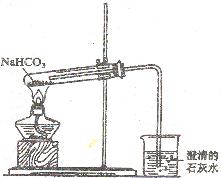 试管中发生的化学反应方程式是:
试管中发生的化学反应方程式是:
②指出该学生设计的装置图的错误之处.并改正(文字说明即可)。
③停止加热时应该怎样操作,为什么?
④烧杯中发生反应的离予方程式是:
(1)饱和NaHCO3溶液(水或NaHCO3也正确)(1分) NaCl的氨溶液 (1分)
(2)洗去晶体吸附的杂质 (2分)
(3)①![]() (2分)
(2分)
②试管内导管太长,伸出活塞即可;试管口应略向上倾斜,“试管夹夹试管太靠近管口”不作为评分要求)(3分)
③先撤除导管,再熄灭酒精灯,否则易使烧杯中的液体倒吸进入热试管使其破裂。(3分)
④![]() (2分)
(2分)

