题目内容
在日常生活中不必对禽流感过于忧虑,由于禽流感病毒对乙醚、氯仿、丙酮、氧化剂等普通消毒剂均敏感,只要注意加强日常消毒即可杀灭病菌。新一代广谱、高效、无污染的饮用水消毒剂ClO2(其中氯元素为+4价,消毒时被还原为-1价)在20世纪后半叶诞生了。ClO2也可作为杀灭环境中禽流感病毒的消毒剂,下列关于ClO2的说法中不正确的是( )A.ClO2可用作消毒剂,是因为它具有强氧化性
B.等质量的ClO2和Cl2,在相同条件下ClO2的消毒效率高
C.现代工业中多用电解法制取ClO2,即![]() +4 H+====4ClO2↑+O2↑+2H2O(条件:电解),ClO2在阳极析出
+4 H+====4ClO2↑+O2↑+2H2O(条件:电解),ClO2在阳极析出
D.将ClO2+Mn2++H2O→MnO2↓+Cl-配平后,H2O的化学计量数为6
解析:本题考查的氧化还原知识、电化学知识、方程式配平、有关计算等均与生活联系紧密。ClO2为氧化型消毒剂,等质量的ClO2和Cl2,在相同条件下ClO2的消毒效率是Cl2的2.63倍。反应![]() +4 H+=====4ClO2↑+O2↑+2H2O中,氯得到电子,氧失去电子,而电解过程中,阳极的氧失去电子,因此,ClO2在阳极析出。配平2ClO2+5Mn2++6H2O→5MnO2↓+12 H++2Cl-。
+4 H+=====4ClO2↑+O2↑+2H2O中,氯得到电子,氧失去电子,而电解过程中,阳极的氧失去电子,因此,ClO2在阳极析出。配平2ClO2+5Mn2++6H2O→5MnO2↓+12 H++2Cl-。
答案:C

练习册系列答案
相关题目
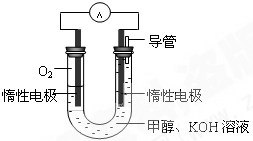 甲醇是重要的化工原料,在日常生活中有着广泛的应用.
甲醇是重要的化工原料,在日常生活中有着广泛的应用. CH3OH(g)△H1
CH3OH(g)△H1 CH3OH(g)+H2O(g)△H2
CH3OH(g)+H2O(g)△H2