题目内容
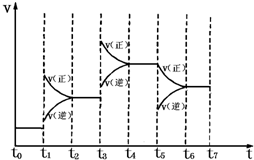 在固定体积的密闭容器中,发生:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ?mol-1,右图表示在时间t0~t7中反应速率与反应过程的曲线图,则容器内氨的百分含量最高的一段时间是(只改变单一的条件)( )
在固定体积的密闭容器中,发生:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ?mol-1,右图表示在时间t0~t7中反应速率与反应过程的曲线图,则容器内氨的百分含量最高的一段时间是(只改变单一的条件)( )分析:t0~t1中正逆反应速率相等,该反应达到平衡状态;
t1~t2中正反应速率大于逆反应速率,平衡向正反应方向移动,
t2~t3中该反应达到平衡状态,氨气百分含量等于t2时;
t3~t4中正反应速率大于逆反应速率,平衡向正反应方向移动,
t4~t5时该反应达到平衡状态,氨气百分含量等于t4时;
t5~t6中正反应速率大于逆反应速率,平衡向正反应方向移动,改变的条件是减少生成物浓度,即氨气的百分含量减少,
t6~t7中正逆反应速率相等,该反应达到平衡状态,氨气百分含量等于t6时.
t1~t2中正反应速率大于逆反应速率,平衡向正反应方向移动,
t2~t3中该反应达到平衡状态,氨气百分含量等于t2时;
t3~t4中正反应速率大于逆反应速率,平衡向正反应方向移动,
t4~t5时该反应达到平衡状态,氨气百分含量等于t4时;
t5~t6中正反应速率大于逆反应速率,平衡向正反应方向移动,改变的条件是减少生成物浓度,即氨气的百分含量减少,
t6~t7中正逆反应速率相等,该反应达到平衡状态,氨气百分含量等于t6时.
解答:解:t0~t1中正逆反应速率相等,该反应达到平衡状态;
t1~t2中正反应速率大于逆反应速率,平衡向正反应方向移动,
t2~t3中该反应达到平衡状态,氨气百分含量等于t2时;
t3~t4中正反应速率大于逆反应速率,平衡向正反应方向移动,
t4~t5时该反应达到平衡状态,氨气百分含量等于t4时;
t5~t6中正反应速率大于逆反应速率,平衡向正反应方向移动,改变的条件是减少生成物浓度,即氨气的百分含量减少,
t6~t7中正逆反应速率相等,该反应达到平衡状态,氨气百分含量等于t6时,
所以氨气百分含量最大时应该是t4~t5一段时间,
故选:C.
t1~t2中正反应速率大于逆反应速率,平衡向正反应方向移动,
t2~t3中该反应达到平衡状态,氨气百分含量等于t2时;
t3~t4中正反应速率大于逆反应速率,平衡向正反应方向移动,
t4~t5时该反应达到平衡状态,氨气百分含量等于t4时;
t5~t6中正反应速率大于逆反应速率,平衡向正反应方向移动,改变的条件是减少生成物浓度,即氨气的百分含量减少,
t6~t7中正逆反应速率相等,该反应达到平衡状态,氨气百分含量等于t6时,
所以氨气百分含量最大时应该是t4~t5一段时间,
故选:C.
点评:本题考查了化学反应速率与平衡图象的关系,会根据正逆反应速率相对大小确定反应方向是解本题关键,难度中等.

练习册系列答案
相关题目
在固定体积的密闭容器中进行如下反应:2AB2(g)+B2(g)?2AB3(g).已知反应过程某一时刻AB2、B2、AB3浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,达到平衡时,浓度可能正确的是( )
| A、AB2、B2分别为0.4mol/L、0.2mol/L | B、AB2为0.25mol/L | C、AB2、AB3均为0.15mol/L | D、AB3为0.4mol/L |
在固定体积的密闭容器中进行如下反应:2SO2(g)+O2(g)?2SO3(g).已知反应过程某一时刻SO2,O2,SO3浓度(mol/L)分别为0.2,0.1,0.2,达到平衡时,浓度可能正确的是( )
| A、SO2为0.4mol/L | B、SO2为0.25mol/L | C、O2为0.2mol/L | D、O2为0mol/L |


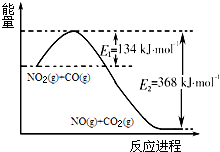 氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.