题目内容
用下列仪器和药品制取氨气,并利用氨气和加热的氧化铜的反应来试验氨气是否具有还原性。通过实验发现:(1)氨具有还原性;(2)氨作还原剂时,生成物中有水;(3)氨作还原剂时,生成物中还有一种无色无味、遇空气不变色的纯净气体。实验中使用的仪器如下:

实验中所需药品:a.消石灰 b.碱石灰 c.浓H2SO4 d.氯化铵 e.氧化铜 f.无水硫酸铜
(1)实验装置的各种仪器的连接顺序按各接口的代码字母填入( )中。并将相应仪器中所装的化学药品的代码字母填入[ ]中(有的仪器可重复使用)
( )接( ),( )接( ),( )接( ),( )接( )
[ ] [ ] [ ] [ ] [ ]
(2)氨与氧化铜反应的化学方程式为 。
(3)实验中可以证明氨具有还原性的最明显的现象是 。
(4)如果实验过程中未发现有水蒸气冷凝后形成的水珠,则证明氨作还原剂时生成物中有水的理由是 。
(5)证明生成的气体不是NO的简易方法是 。
答案:
解析:
提示:
解析:
| (1)(A)接(F),(G)接(B),(C)接(F),(G)接(D)。
[a d] [b] [e] [f] [c] (2)2NH3+3CuO (3)黑色的氧化铜变为光亮的红色 (4)白色的无水硫酸铜粉末变成蓝色 (5)将生成的无色无味气体与空气接触,不变色,证明不是NO
|
提示:
| 本实验的基本思路是:制气→净化→反应→鉴别→吸收。用a消石灰和d氯化铵固体混合加热制氨,故选用A装置。由于氨是碱性气体,应该用盛有碱性干燥剂——碱石灰的U形管进行干燥,然后通入直玻璃管与氧化铜进行反应。,黑色粉末变成光亮的红色这一明显现象证明氨具有还原性,将氧化铜还原为铜。为了证明产物中有水,将反应完的气体通过盛有无水硫酸铜的U形管中,白色粉末变蓝,证明氨作还原剂时生成物中有水,最后用浓硫酸吸收未反应的氨以防止污染空气。所以仪器的连接顺序为:(A)接(F),(G)接(B),(C)接(F),(G)接(D)。
2NH3+3CuO |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
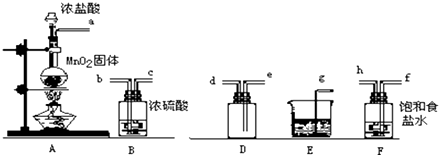
 实验室用下列仪器和药品制取并收集干燥纯净的氯气.
实验室用下列仪器和药品制取并收集干燥纯净的氯气.

 :
:
 A 。
A 。