题目内容
2SO2(g)+O2(g)?2SO3(g);△H=-196.6kJ/mol.在一定温度下,向一个容积不变的容器中,通入3mol SO2和2mol O2及固体催化剂,使之反应.平衡时容器内气体压强为起始时的90%.此时
(1)加入3mol SO2和2mol O2发生反应,达到平衡时,放出的热量为
(2)保持同一反应温度,在相同的容器中,将起始物质的量改为amol SO2、bmol O2、cmol SO3(g)及固体催化剂,欲使起始时反应表现为向正反应方向进行,且平衡时SO3的体积分数为2/9,a的取值范围是
(3)保持同一反应温度,在相同的容器中,将起始物质的量改为3mol SO2、6mol O2、3mol SO3(g)及固体催化剂,则平衡
(1)加入3mol SO2和2mol O2发生反应,达到平衡时,放出的热量为
98.3kJ
98.3kJ
.(2)保持同一反应温度,在相同的容器中,将起始物质的量改为amol SO2、bmol O2、cmol SO3(g)及固体催化剂,欲使起始时反应表现为向正反应方向进行,且平衡时SO3的体积分数为2/9,a的取值范围是
2<a≤3
2<a≤3
.(3)保持同一反应温度,在相同的容器中,将起始物质的量改为3mol SO2、6mol O2、3mol SO3(g)及固体催化剂,则平衡
不
不
移动.(填“正向、不、逆向或 无法确定是否)分析:(1)根据压强之比等于物质的量之比计算平衡时混合气体总的物质的量,再利用差量法计算参加反应的二氧化硫的物质的量,结合热化学方程式计算放出的热量;
(2)根据(1)计算可知,原平衡时SO3的体积分数为
=
,将起始物质的量改为amol SO2、bmol O2、cmol SO3(g)及固体催化剂,平衡时SO3的体积分数为
,则与原平衡为等效平衡,计算原平衡时二氧化硫的物质的量,欲使起始时反应表现为向正反应方向进行,则a应大于原平衡状态时二氧化硫的物质的量,结合极限法判断;
(3)假定体积为VL,利用三段式计算原平衡时各组分的物质的量,进而计算平衡常数,将起始物质的量改为3mol SO2、6mol O2、3mol SO3(g)及固体催化剂,计算此时的浓度商,与平衡常数比较判断反应进行方向.
(2)根据(1)计算可知,原平衡时SO3的体积分数为
| 1mol |
| 4.5mol |
| 2 |
| 9 |
| 2 |
| 9 |
(3)假定体积为VL,利用三段式计算原平衡时各组分的物质的量,进而计算平衡常数,将起始物质的量改为3mol SO2、6mol O2、3mol SO3(g)及固体催化剂,计算此时的浓度商,与平衡常数比较判断反应进行方向.
解答:解:(1)由题意气体压强为起使时的90%,则反应后总的物质的量为起使时的90%,平衡时总物质的量为(3mol+2mol)×90%=4.5mol,则平衡时各组成物质的量变化为:
2SO2+O2?2SO3 物质的量减少△n
2 1 2 1
1mol 0.5mol 1mol (3mol+2mol)-4.5mol=0.5mol
此时放出的热量为196.6KJ×
=98.3KJ,
故答案为:98.3;
(2)原平衡时SO3的体积分数为
=
,将起始物质的量改为amol SO2、bmol O2、cmol SO3(g)及固体催化剂,平衡时SO3的体积分数为
,则与原平衡为等效平衡,则a+c=3 b+0.5c=2,由(1)计算可知,平衡时二氧化硫的物质的量为3mol-1mol=2mol,欲使起始时反应表现为向正反应方向进行,则2<a≤3,
故答案为:2<a≤3;
(3)由题意气体压强为起使时的90%,则反应后总的物质的量为起使时的90%,平衡时总物质的量为(3mol+2mol)×90%=4.5mol,则平衡时各组成物质的量变化为:
2SO2+O2?2SO3
开始(mol):3 2 0
变化(mol):1 0.5 1
平衡(mol):2 1.5 1
假定体积为VL,则k=
=
,将起始物质的量改为3mol SO2、6mol O2、3mol SO3(g)及固体催化剂,此时的浓度商Qc=
=
,等于平衡常数,处于平衡状态,平衡不移动,
故答案为:不.
2SO2+O2?2SO3 物质的量减少△n
2 1 2 1
1mol 0.5mol 1mol (3mol+2mol)-4.5mol=0.5mol
此时放出的热量为196.6KJ×
| 0.5mol |
| 1mol |
故答案为:98.3;
(2)原平衡时SO3的体积分数为
| 1mol |
| 4.5mol |
| 2 |
| 9 |
| 2 |
| 9 |
故答案为:2<a≤3;
(3)由题意气体压强为起使时的90%,则反应后总的物质的量为起使时的90%,平衡时总物质的量为(3mol+2mol)×90%=4.5mol,则平衡时各组成物质的量变化为:
2SO2+O2?2SO3
开始(mol):3 2 0
变化(mol):1 0.5 1
平衡(mol):2 1.5 1
假定体积为VL,则k=
(
| ||||
(
|
| V |
| 6 |
(
| ||||
(
|
| V |
| 6 |
故答案为:不.
点评:本题为化学平衡和反应热综合试题,试题难度较大,(3)中反应进行方向判断为易错点、难点,注意掌握化学平衡常数的运用.

练习册系列答案
相关题目
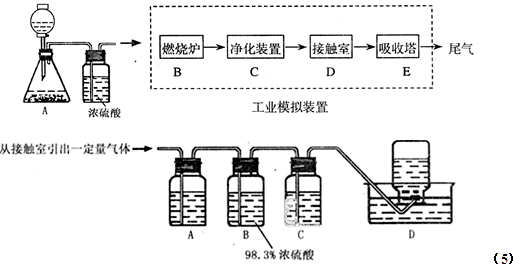
 (2009?丹东模拟)请根据工业制硫酸的有关知识回答下列问题:
(2009?丹东模拟)请根据工业制硫酸的有关知识回答下列问题: