题目内容
16.有aW、bX、cY、dZ四种短周期元素,已知d-c=c-b=b-a=5,且W、X、Y的最外层电子数总和大于Z的最外层电子数.下列说法不正确的是( )| A. | W元素的单质常温下是气体 | |
| B. | X是蛋白质的组成元素之一 | |
| C. | Y元素的单质能与冷水发生剧烈反应 | |
| D. | Z元素的气态氢化物的水溶液呈酸性 |
分析 aW、bX、cY、dZ四种短周期元素,已知d-c=c-b=b-a=5,则d-a=15,如a=1,则W为H元素,X为C元素,Y为Na元素,Z为S元素,W、X、Y的最外层电子数总和为1+1+4-6,等于Z的最外层电子数,不符合题意,如a=2,为He元素,则b=7,为N元素,c=12,为Mg元素,Z为Cl元素,满足W、X、Y的最外层电子数总和大于Z的最外层电子数,如a=3,为Li元素,则b=8,为O元素,Y为Al元素,Z为Ar元素,满足W、X、Y的最外层电子数总和大于Z的最外层电子数,以此解答该题.
解答 解:由以上分析可知W为He或Li元素,X为N或O元素,Y为Mg或Al元素,Z为Cl 或Ar元素.
A.如W为He,则常温下为气体,故A正确;
B.X为N或O元素,是蛋白质的组成元素之一,故B正确;
C.Y为Mg或Al元素,与冷水都不反应,故C错误;
D.如Z为Cl元素,则气态氢化物的水溶液呈酸性,为盐酸,故D正确.
故选C.
点评 本题考查原子结构与元素周期律,为高频考点,把握短周期原子序数关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
6.下列哪一种是sp2杂化轨道的电子云轮廓图( )
| A. |  | B. |  | C. |  | D. |  |
7.反应A+3B═2C+2D在四种不同情况下的反应速率分别为:
①v(A)=0.15mol•(L•s)-1;
②v(B)=0.6mol•(L•s)-1;
③v(C)=6mol•(L•min)-1;
④v(D)=0.45mol•(L•s)-1.
则反应进行的快慢为( )
①v(A)=0.15mol•(L•s)-1;
②v(B)=0.6mol•(L•s)-1;
③v(C)=6mol•(L•min)-1;
④v(D)=0.45mol•(L•s)-1.
则反应进行的快慢为( )
| A. | ④>②>①>③ | B. | ③>①>②>④ | C. | ①>②>③>④ | D. | ③>②>④>① |
4.某溶液只含下表离子中的几种,且各离子的物质的量浓度相等(不考虑水的电离与离子水解).
某同学进行了如下实验(必要时可加热):

下列说法正确的是( )
| 阳离子 | K+、NH4+、Fe2+、Mg2+、Cu2+ |
| 阴离子 | OH-、Cl-、CO32-、SO42- |

下列说法正确的是( )
| A. | 滤液A中可能含有K+ | |
| B. | 沉淀B中一定含有Mg(OH)2 | |
| C. | 由沉淀A推断原溶液中一定含有SO42- | |
| D. | 原溶液中只含有NH4+、Fe2+、Cl-、SO42- |
11.下列变化中,吸收的热量用于克服分子间作用力的是( )
| A. | 加热氯化钠使之熔化 | B. | 加热二氧化硅使之熔化 | ||
| C. | 液溴受热变成溴蒸气 | D. | 加热碘化氢使之分解 |
9.实验室制备下列气体时,只能用排水法收集的气体是( )
| A. | H2 | B. | NO | C. | NO2 | D. | CO2 |
6.某有机物的结构简式为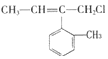 ,则该物质不能发生的反应有( )
,则该物质不能发生的反应有( )
 ,则该物质不能发生的反应有( )
,则该物质不能发生的反应有( )| A. | 加成反应 | B. | 氧化反应 | C. | 取代反应 | D. | 消去反应 |

