题目内容
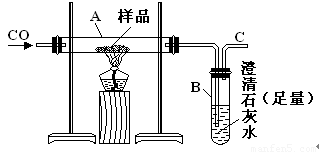
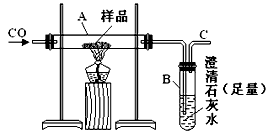
(10分)实验室可以用下图装置进行CO还原赤铁矿(主要成分为Fe2O3)并测定其中铁的含量的实验(假设杂质不参与反应)。请回答下列问题:

(1)该实验中炼铁的方法是________(填字母)。
A.热分解法 B.热还原法
C.电解法 D.湿法冶金
(2)实验开始后,B中的现象是____________________,A中反应的化学方程式是________________________________________________________。
(3)写出铝和Fe2O3 反应的化学方程式 演示实验引发该反应的方法是
(4)若样品的质量为3.6 g,通入足量的CO充分反应后,B增重2.64 g,则样品中铁的质量分数为_____ _ (结果保留一位小数)。
(1)B (2)有白色沉淀生成;Fe2O3+3CO2Fe+3CO2
(3) Fe2O3+2Al2Fe+Al2O3 在铝热剂上放KClO3,插上镁条并将镁条点燃
(4)62.2%
【解析】(1)CO具有还原性,答案选B。
(2)CO的氧化产物是CO2,CO2能和氢氧化钙溶液反应生成白色沉淀。CO还原氧化铁的方程式为Fe2O3+3CO2Fe+3CO2。
(3)铝也具有还原性, 能发生铝热反应,方程式为 Fe2O3+2Al2Fe+Al2O3。
(4)B增重2.64 g,说明CO2是2.64g,物质的量是0.06mol。因此根据方程式可知生成铁是0.04mol,所以样品中铁的质量分数为0.04mol×56g/mol÷3.6g×100%=62.2%。

(10分)实验室可以用下图装置进行CO还原赤铁矿(主要成分为Fe2O3)并测定其中铁的含量的实验(假设杂质不参与反应)。请回答下列问题: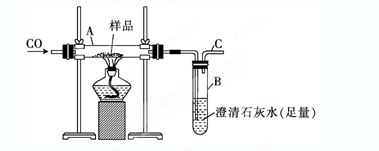
(1)该实验中炼铁的方法是________(填字母)。
| A.热分解法 | B.热还原法 |
| C.电解法 | D.湿法冶金 |
(3)写出铝和Fe2O3 反应的化学方程式 演示实验引发该反应的方法是
(4)若样品的质量为3.6 g,通入足量的CO充分反应后,B增重2.64 g,则样品中铁的质量分数为_____ _ (结果保留一位小数)。