题目内容
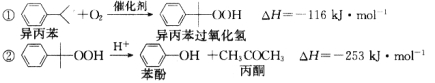
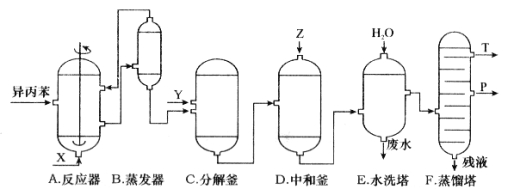
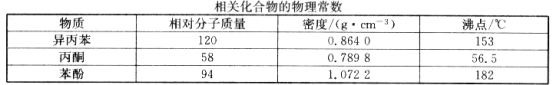
【题目】下列事实不能用勒夏特列原理解释的是( )
A.光照新制的氯水时,颜色变浅,溶液的酸性增强
B.打开可乐瓶,有大量气泡从溶液中冒出
C.I2(g)+H2(g)![]() 2HI(g)的平衡体系,加压后颜色变深
2HI(g)的平衡体系,加压后颜色变深
D.高压有利于SO2和O2反应生成SO3
【答案】C
【解析】
试题分析:A.氯水中存在平衡Cl2+H2O![]() HClO+H++Cl-,光照HClO分解,溶液中HClO浓度降低,平衡向生成HClO方向移动,酸性增强,可用勒夏特列原理解释,A不选;B.开启可乐瓶后,瓶中马上泛起大量泡沫,是压强对其影响导致的,属于可逆过程,B不选;C.可逆反应为I2(g)+H2(g)
HClO+H++Cl-,光照HClO分解,溶液中HClO浓度降低,平衡向生成HClO方向移动,酸性增强,可用勒夏特列原理解释,A不选;B.开启可乐瓶后,瓶中马上泛起大量泡沫,是压强对其影响导致的,属于可逆过程,B不选;C.可逆反应为I2(g)+H2(g)![]() 2HI(g),增大压强I2的浓度增大,颜色加深,反应前后气体的体积不发生变化,增大压强平衡不移动,颜色加深是体积改变的原因,不能用用勒夏特列原理解释,C符合题意;D.反应为O2(g)+2SO2(g)
2HI(g),增大压强I2的浓度增大,颜色加深,反应前后气体的体积不发生变化,增大压强平衡不移动,颜色加深是体积改变的原因,不能用用勒夏特列原理解释,C符合题意;D.反应为O2(g)+2SO2(g)![]() 2SO3正反应为气体体积减小的放热反应,增大压强平衡向体积减小的方向移动,所以可以用平衡移动原理解释,D不选;答案选C。
2SO3正反应为气体体积减小的放热反应,增大压强平衡向体积减小的方向移动,所以可以用平衡移动原理解释,D不选;答案选C。

【题目】(1)实验室需要450 mL 0.02 mol/L酸性KMnO4标准溶液,现有仪器:
① 托盘天平 ② 玻璃棒 ③ 药匙 ④ 200mL烧杯 ⑤ 量筒,还需要 玻璃仪器才能完成配制,需称量KMnO4固体 g。
(2)下列操作会使配制的KMnO4溶液浓度偏大的是 (填写编号,假设其他操作均正确)。
A.没有冷却至室温就转移液体到容量瓶并完成定容 |
B.使用容量瓶配制溶液,定容时,俯视刻度线 |
C.没有用蒸馏水洗涤烧杯2-3次,并将溶液移入容量瓶中 |
D.容量瓶刚用蒸馏水洗净,没有烘干就用来配制溶液 |
E.定容时,滴加蒸馏水,不慎液面略高于刻度线,吸出少量水使凹液面最低点与刻度线相切
(3)配平下面的方程式(将有关的化学计量数填入答题卡的横线上):
□KMnO4+□H2C2O4+□H2SO4——□MnSO4+□K2SO4+□H2O+□CO2↑
(4)人体血液里Ca2+的浓度一般以mg/cm3为单位。为测定血液样品中Ca2+的浓度,抽取血样20.00 mL,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用上述标准0.02 mol/L 酸性KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗13.00 mL酸性 KMnO4溶液,请计算血液样品中Ca2+的浓度为_________mg/cm3(保留到小数点后两位)。