题目内容
工业上制金刚砂(SiC)的化学方程式如下:SiO2+3C![]() SiC+2CO↑在这个氧化还原反应中,氧化剂与还原剂物质的量之比是( )
SiC+2CO↑在这个氧化还原反应中,氧化剂与还原剂物质的量之比是( )
A.1∶2 B.2∶1 C.1∶1 D.3∶5
答案:A
解析:
解析:
分析该反应的电子转移情况时: 可知C在此反应中既做氧化剂,又做还原剂,且得电子的碳物质的量与失电子的碳的物质的量之比为1∶2,亦即氧化剂与还原剂的物质的量之比为1∶2。
|

练习册系列答案
相关题目
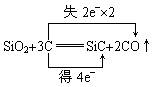
 SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为 。
SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为 。 SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为 。
SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为 。 SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为 。
SiC+2CO。在该反应中氧化剂和还原剂的物质的量比为 。
