题目内容
15.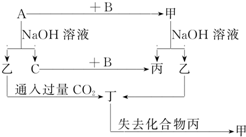 由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有图示的转换关系,已知C为密度最小的气体.
由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有图示的转换关系,已知C为密度最小的气体.根据图示转化关系回答:
(1)若甲是电解质?写出下列物质的化学式:甲Al2O3,丁Al(OH)3?写出乙与过量CO2反应的离子方程式:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-?
(2)若甲是非电解质?写出下列物质的化学式:甲SiO2,乙Na2SiO3?
分析 (1)C为密度最小的气体,则C是H2,金属A和氢氧化钠溶液反应生成乙和氢气,中学阶段学习的能和氢氧化钠溶液反应生成氢气的金属只有Al,所以A是Al,乙是NaAlO2,铝和单质B反应生成甲,甲中含有铝元素,甲是电解质,能和氢氧化钠溶液,则甲是Al2O3,B是O2,氧化铝和氢氧化钠溶液反应生成偏铝酸钠和水,则丙是H2O,偏铝酸钠和二氧化碳反应生成氢氧化铝和碳酸氢钠,丁失去水生成氧化铝,则丁是Al(OH)3;
(2)C为密度最小的气体,则C是H2,甲为非电解质,则非金属A和氢氧化钠溶液反应生成乙和氢气,中学阶段学习的能和氢氧化钠溶液反应生成氢气的非金属只有Si,然后结合发生的转化反应来解答.
解答 解:(1)C为密度最小的气体,则C是H2,金属A和氢氧化钠溶液反应生成乙和氢气,中学阶段学习的能和氢氧化钠溶液反应生成氢气的金属只有Al,所以A是Al,乙是NaAlO2,铝和单质B反应生成甲,甲中含有铝元素,甲是电解质,能和氢氧化钠溶液,则甲是Al2O3,B是O2,氧化铝和氢氧化钠溶液反应生成乙为偏铝酸钠,则丙是H2O,偏铝酸钠和二氧化碳反应生成氢氧化铝和碳酸氢钠,丁失去水生成氧化铝,则丁是Al(OH)3,乙与过量CO2反应的离子方程式为AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-,故答案为:Al2O3;Al(OH)3;AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-;
(2)C为密度最小的气体,则C是H2,甲为非电解质,则非金属A和氢氧化钠溶液反应生成乙和氢气,中学阶段学习的能和氢氧化钠溶液反应生成氢气的非金属只有Si,甲为SiO2,B是O2,丙为水,乙为Na2SiO3,故答案为:SiO2;Na2SiO3.
点评 本题考查无机物的推断,为高频考点,把握Si和Al的化合物性质及图中转化关系为解答的关键,侧重分析、推断及应用能力的考查,综合性较强,题目难度中等.

| A. | PH3 | B. | H2S | C. | HCl | D. | HBr |
| A. | 含有离子键的化合物一定是离子化合物 | |
| B. | 同种非金属元素间不可能形成离子键 | |
| C. | 非金属元素间不可能形成离子化合物 | |
| D. | 分子中一定存在共价键 |
①将乙酸和乙醇混合加热制乙酸乙酯
②苯和浓溴水反应制溴苯
③CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型
④用2mL0.1mol/L的CuSO4溶液和2mL0.1mol/L的NaOH溶液混合,然后加入几滴乙醛,加热,根据是否产生红色沉淀来检验醛基.
| A. | ①②③④ | B. | ①③④ | C. | ①②③ | D. | ②③④ |
| A. | NaHCO3 | B. | C2H6 | C. | HCHO | D. | CH3OH |
| A. | 水玻璃可用作木材防火剂 | B. | 用大量的二氧化硫作食品漂白剂 | ||
| C. | 硅可用于制造太阳能电池 | D. | 食醋可作除去保温瓶的水垢 |
 .
. .
. .元素D在元素周期表中的位置是第三周期第VIIA族.
.元素D在元素周期表中的位置是第三周期第VIIA族.
 .
. (写出结构简式).
(写出结构简式).