题目内容
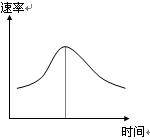
氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图所示.已知这个反应速率随着溶液中c(H+)增大而加快.

(1)反应开始速率加快的原因是________.
(2)反应后期速率下降的原因是________.
答案:
解析:
解析:
|
答案:(1)2KClO3+6NaHSO3 (2)H2SO4和NaHSO3之间的反应使H+和 思路解析:问题(1)作为已知考虑,开始时反应速率的加快,有哪些因素能引起溶液中反应速率的加快呢?①增大浓度,②增压,③升温,④加正催化剂.联系题意可排除②④,由于题意中不涉及热量变化,故不需考虑③;接下来考虑①,但题中无外加物,所以只考虑c(H+)的变化,KClO3→Cl-,NaHSO3→ |

练习册系列答案
相关题目