题目内容
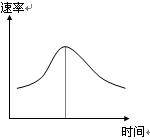
氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图所示,已知这个反应速率随着溶液中c(H+)增大而加快。
(1)反应开始时,反应速率加快的原因是_____________________________________________。
(2)反应后期,反应速率又下降的原因是_____________________________________________。
解析:我们知道,下列因素能引起化学反应速率加快:①增加浓度;②增大气体的压强,从而缩小体积;③升温;④加正催化剂。依题意可首先排除②和④;由于题意中不涉及供热及热量变化,故不需要考虑③;题中没有外加物质,所以也不需要考虑①。因此,只考虑c(H+)的变化对化学反应速率的影响。
答案:(1)反应开始时,2KClO3+6NaHSO3![]() 3Na2SO4+2KCl+3H2SO4,由于生成较多的H2SO4,则c(H+)增大,必然导致化学反应速率加快
3Na2SO4+2KCl+3H2SO4,由于生成较多的H2SO4,则c(H+)增大,必然导致化学反应速率加快
(2)反应后期,H2SO4和NaHSO3反应,使c(H+)和c(![]() )均减小,则化学反应速率又减小
)均减小,则化学反应速率又减小

练习册系列答案
相关题目