题目内容
已知:H2(g)+ O2(g)=H2O(g),反应过程中能量变化如图所示:
O2(g)=H2O(g),反应过程中能量变化如图所示:请回答下列问题:
(1)a、b、c分别代表的意义
a.______,b.______,c.______;
(2)该反应是______反应(填“放热”或“吸热”),△H______0(填“>”、“<”或“=”);
(3)若已知2H2O(g)+O2(g)=2H2O(g)△H1=-Q1kJ?mol-1;
2H2O(g)+O2(g)=2H2O(l)△H2=-Q2kJ?mol-1,
则△H1______△H2,Q1______Q2(填“>”“<”或“=”).

【答案】分析:(1)图象分析可知,化学反应的热效应实质是断裂化学键吸收的热量减去形成化学键放出的热量,所以a表示的是破坏1molH2和 mol O2中化学键所吸收的能量,b表示的是由2mol H和1mol O形成1mol H2O(g)所放出的能量;c表示的是反应的焓变即反应热;
mol O2中化学键所吸收的能量,b表示的是由2mol H和1mol O形成1mol H2O(g)所放出的能量;c表示的是反应的焓变即反应热;
(2)依据反应的能量守恒和反应物生成物的能量高低分析判断;
解答:解:(1)图象分析可知,化学反应的热效应实质是断裂化学键吸收的热量减去形成化学键放出的热量,所以a表示的是破坏1molH2和 mol O2中化学键所吸收的能量,b表示的是由2mol H和1mol O形成1mol H2O(g)所放出的能量;c表示的是反应的焓变即反应热;
mol O2中化学键所吸收的能量,b表示的是由2mol H和1mol O形成1mol H2O(g)所放出的能量;c表示的是反应的焓变即反应热;
故答案为:a.破坏1molH2和 mol O2中化学键所吸收的能量;b.由2mol H和1mol O形成1mol H2O(g)所放出的能量;c.反应热;
mol O2中化学键所吸收的能量;b.由2mol H和1mol O形成1mol H2O(g)所放出的能量;c.反应热;
(2)反应物的能量高于生成物,反应是放热反应,焓变小于0;故答案为:放热;<;
(3)若已知2H2(g)+O2(g)=2H2O(g)△H1=-Q1kJ?mol-1;2H2(g)+O2(g)=2H2O(l)△H2=-Q2kJ?mol-1,
生成气态水放出的热量数值小于生成液态水放出的热量数值,即Q1<Q2;所以焓变△H1>△H2;
故答案为:><;
点评:本题考查了反应的热量变化的依据和含义,图象分析、反应实质、能量守恒是解题关键,题目难度中等.
 mol O2中化学键所吸收的能量,b表示的是由2mol H和1mol O形成1mol H2O(g)所放出的能量;c表示的是反应的焓变即反应热;
mol O2中化学键所吸收的能量,b表示的是由2mol H和1mol O形成1mol H2O(g)所放出的能量;c表示的是反应的焓变即反应热;(2)依据反应的能量守恒和反应物生成物的能量高低分析判断;
解答:解:(1)图象分析可知,化学反应的热效应实质是断裂化学键吸收的热量减去形成化学键放出的热量,所以a表示的是破坏1molH2和
 mol O2中化学键所吸收的能量,b表示的是由2mol H和1mol O形成1mol H2O(g)所放出的能量;c表示的是反应的焓变即反应热;
mol O2中化学键所吸收的能量,b表示的是由2mol H和1mol O形成1mol H2O(g)所放出的能量;c表示的是反应的焓变即反应热;故答案为:a.破坏1molH2和
 mol O2中化学键所吸收的能量;b.由2mol H和1mol O形成1mol H2O(g)所放出的能量;c.反应热;
mol O2中化学键所吸收的能量;b.由2mol H和1mol O形成1mol H2O(g)所放出的能量;c.反应热;(2)反应物的能量高于生成物,反应是放热反应,焓变小于0;故答案为:放热;<;
(3)若已知2H2(g)+O2(g)=2H2O(g)△H1=-Q1kJ?mol-1;2H2(g)+O2(g)=2H2O(l)△H2=-Q2kJ?mol-1,
生成气态水放出的热量数值小于生成液态水放出的热量数值,即Q1<Q2;所以焓变△H1>△H2;
故答案为:><;
点评:本题考查了反应的热量变化的依据和含义,图象分析、反应实质、能量守恒是解题关键,题目难度中等.

练习册系列答案
相关题目
 已知:H2(g)+
已知:H2(g)+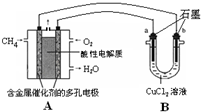 (2013?焦作一模)开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的.
(2013?焦作一模)开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的. 已知:H2(g)+
已知:H2(g)+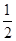 O2(g)=H2 O(g) △H=-241.8kJ·mol-1
O2(g)=H2 O(g) △H=-241.8kJ·mol-1 2NO(g)
△H
2NO(g)
△H 0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在1.0 L密闭容器内经过5s反应达到平衡,测得NO为8.0×10-4 mol。
0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在1.0 L密闭容器内经过5s反应达到平衡,测得NO为8.0×10-4 mol。 2CO2(g)+N2(g) 中,NO的浓度
2CO2(g)+N2(g) 中,NO的浓度