��Ŀ����
ij�о���ѧϰС��̽��NO3-�ڲ�ͬ�����е������ԡ�
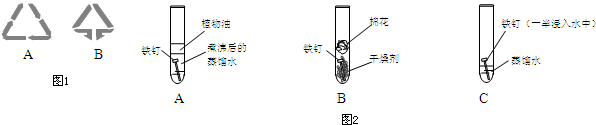
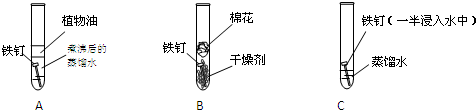
(1)ʵ��һ��
���Թ�a��b�о������Ũ�ȡ��������NaNO3��Һ�͵�������ͭƬ�����ȣ�����������
�� ���Թ�a�м���V mL NaOH��Һ�����ȣ�����������
�����Թ�b�м���V mLϡH2SO4�����ȣ��ɹ۲쵽��������___________��
ʵ��һ��Ŀ����___________��
(2)ʵ�����������ͼװ��̽����ͬŨ��HNO3�������ԡ�
����֪������ָ��ƫת�����ǵ����ƶ�����ͭ��������ͬʱ����ŨHNO3�У��۲쵽������ָ��ָ��ͭ����Ѹ�ٷ�ת��ָ��ƫ����һ�ˣ���ʱ������_________���������������ָ�뷴ת��ԭ����__________
(1)ʵ��һ��
���Թ�a��b�о������Ũ�ȡ��������NaNO3��Һ�͵�������ͭƬ�����ȣ�����������
�� ���Թ�a�м���V mL NaOH��Һ�����ȣ�����������
�����Թ�b�м���V mLϡH2SO4�����ȣ��ɹ۲쵽��������___________��
ʵ��һ��Ŀ����___________��
(2)ʵ�����������ͼװ��̽����ͬŨ��HNO3�������ԡ�
����֪������ָ��ƫת�����ǵ����ƶ�����ͭ��������ͬʱ����ŨHNO3�У��۲쵽������ָ��ָ��ͭ����Ѹ�ٷ�ת��ָ��ƫ����һ�ˣ���ʱ������_________���������������ָ�뷴ת��ԭ����__________

�ڽ�ŨHNO3��ΪϡHNO3�۲쵽������ָ��ָ��ͭ����ʱ������Ӧʽ��_______________��
(1)��ͭ�ܽ⣬������ɫ���壬��Һ����ɫ����ɫ��̽��NO3-���ᡢ������Һ�е�������
(2)����������Ũ������Ѹ����������������γ����ܵ�����Ĥ���谭���ڲ�����һ����Ũ���ᷴӦ������Ũ�����жۻ�������NO3-+4H++3e-=NO��+2H2O
(2)����������Ũ������Ѹ����������������γ����ܵ�����Ĥ���谭���ڲ�����һ����Ũ���ᷴӦ������Ũ�����жۻ�������NO3-+4H++3e-=NO��+2H2O

��ϰ��ϵ�д�
 ��������״Ԫ��ϵ�д�
��������״Ԫ��ϵ�д� �ƸԿ�����ҵ��ϵ�д�
�ƸԿ�����ҵ��ϵ�д� ��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
�����Ŀ
 Fe2++Ag+����ش��������⣺
Fe2++Ag+����ش��������⣺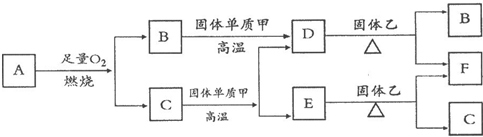

 CO2��SO2��NOx�ǶԻ���Ӱ��ϴ�����壬���ƺ�����CO2��SO2��NOx�ǽ������ЧӦ����������⻯ѧ��������Ч;����
CO2��SO2��NOx�ǶԻ���Ӱ��ϴ�����壬���ƺ�����CO2��SO2��NOx�ǽ������ЧӦ����������⻯ѧ��������Ч;���� CO+3H2
CO+3H2