题目内容
(10分)有机物A常用于食品行业。已知9.0 g A在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4 g和13.2 g,经检验剩余气体为O2。
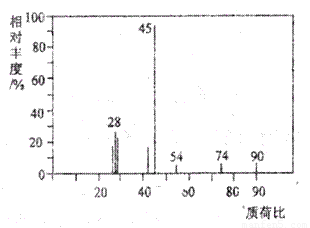
(1)A分子的质谱图如下图所示,从图中可知其相对分子质量是90,则A的分子式是______________________。

(2)A能与NaHCO3溶液发生反应,A一定含有的官能团名称是__________________。
(3)A分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则A的结构简式是_________________________________。
(4)0.1 mol A与足量Na反应,在标准状况下产生H2的体积是__________L。
(5)A在一定条件下可聚合得到一种聚酯,用于制造手术缝合线,其反应的化学方程式是___________________________________________________________________。
(1)C3H6O3
(2)羧基 (3)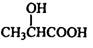 (4)2.24
(4)2.24
(5)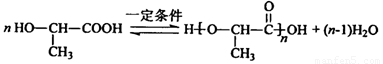
【解析】(1)浓硫酸增重的质量就是水的质量,即水是5.4g,物质的量是0.3mol。碱石灰增加的质量是CO2恶质量,所以CO2的物质的量是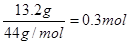 。因此有机物A中氧原子的物质的量
。因此有机物A中氧原子的物质的量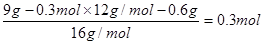 ,所以有机物A中碳、氢、氧的原子个数之比是1︰2︰1。又因为A的相对分子质量是90,所以A的分子式为C3H6O3。
,所以有机物A中碳、氢、氧的原子个数之比是1︰2︰1。又因为A的相对分子质量是90,所以A的分子式为C3H6O3。
(2)A能与NaHCO3溶液发生反应,所以A一定含有的官能团是羧基。
(3)根据A的核磁共振氢谱可判断,A的结构简式为CH3CHOHCOOH。
(4)因为A中含有1个羟基和1个羧基,所以1molA能生成1mol氢气。
(5)A中含有醇羟基和羧基,可发生缩聚反应,生成聚酯,反应式为
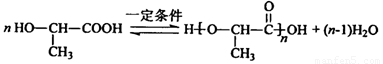

 阅读快车系列答案
阅读快车系列答案 有机物A常用于食品行业.已知9.0g A在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2.
有机物A常用于食品行业.已知9.0g A在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2.