题目内容
符合下列各种条件的溶液中,各组离子可能大量共存的是
- A.pH=0的溶液中:Na+、NH4+、CO32-、Cl-
- B.Br-不能大量存在的溶液中:Mg2+、Ca2+、Cl-、NO3-
- C.加入铝粉后能产生氢气的溶液中:Cu2+、Ba2+、Cl-、NO3-
- D.常温下水电离出的c(H+)=10-4的溶液中:Fe3+、K+、ClO-、SO42-
分析:A.pH=0的溶液中H+与CO32-反应;
B.离子之间不发生反应;
C.加入铝粉后能产生氢气的溶液可能为酸或碱的溶液;
D.常温下水电离出的c(H+)=10-4的溶液,水的电离受到促进,溶液中存在能水解的离子.
解答:A.pH=0的溶液中H+与CO32-反应生成水和二氧化碳,则不能共存,故A错误;
B.该组离子之间不发生反应,则能够大量共存,故B正确;
C.加入铝粉后能产生氢气的溶液可能为酸或碱的溶液,酸溶液中不生成氢气,则不符合题意,而碱溶液与Cu2+结合生成沉淀,则不能共存,故C错误;
D.常温下水电离出的c(H+)=10-4的溶液,水的电离受到促进,溶液中存在能水解的离子,则会与Fe3+或ClO-相互促进水解而不能共存,故D错误;
故选B.
点评:本题考查离子的共存问题,明确信息的应用是解答本题的关键,并利用离子之间的反应来解答,注意D选项是解答的难点.

实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。化工行业的发展必须符合国家节能减排的总体要求,依靠理论知识做基础。试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为: 它所对应的化学反应为:_____________________________
它所对应的化学反应为:_____________________________
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)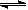 CH3OH(g);ΔH=-90.8 kJ/mol
CH3OH(g);ΔH=-90.8 kJ/mol
②2CH3OH(g)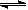 CH3OCH3(g)+H2O(g);ΔH=-23.5 kJ/mol
CH3OCH3(g)+H2O(g);ΔH=-23.5 kJ/mol
③CO(g)+ H2O(g)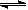 CO2(g)+H2(g);ΔH=-41.3 kJ/mol
CO2(g)+H2(g);ΔH=-41.3 kJ/mol
总反应:3H2(g)+3CO(g)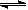 CH3OCH3(g)+CO2(g)的ΔH=__________ ,
CH3OCH3(g)+CO2(g)的ΔH=__________ ,
二甲醚(CH3OCH3)直接作燃料电池具有启动快,效率高等优点,若电解质为酸性,该电池的负极反应为_____________________________。
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g) ? H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
? H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
该反应的正反应方向是_________反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,CO的平衡转化率为:________。
(4)从氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等。对反应? N2O4(g)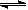 2NO2(g)? △H>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是___________。
2NO2(g)? △H>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是___________。

A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
E.A、C两点的化学平衡常数:A>C
(5)NO2可用氨水吸收生成NH4NO3 。25℃时,将m mol NH4NO3溶于水,溶液显酸性,向该溶液滴加n L氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将______(填”正向”“不”或“逆向”)移动,所滴加氨水的浓度为_______mol·L-1。(NH3·H2O的电离平衡常数取Kb=2X10-5 mol·L-1)
(6)某科研单位利用原电池原理,用SO2和O2来制备硫酸,装置如右图,电极为多孔的材料能吸附气体,同时也能使气体与电解质溶液充分接触.

①溶液中H+的移动方向由______ 极到______极;(用A、B表示)
②B电极的电极反应式为__________________________。