题目内容
有人设计将两根Pt丝作电极插入KOH溶液中,然后在两极上分别通过甲烷和氧气而构成燃料电池.该电池中反应的化学方程式为 ,则关于此燃料电池的下列说法错误的是(1个电子所带电量为
,则关于此燃料电池的下列说法错误的是(1个电子所带电量为 )
)
[ ]
A.通过甲烷的电极为电池的负极,通过氧气的电极为正极
B.在标准状况下,每消耗5.6L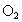 ,可向外提供约
,可向外提供约 的电量
的电量
C.通过甲烷电极的电极反应为
D.放电一段时间后,溶液的pH升高
答案:D
解析:
解析:
|
解析:原电池的正极发生还原反应,负极发生氧化反应.这里的燃料电池电极反应为:负极 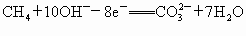 ,正极 ,正极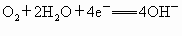 . .
由此可见 A、C正确.由正极电极反应可知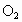 ~ ~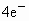 ,所以5.6L ,所以5.6L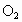 消耗时可向外提供电量为 消耗时可向外提供电量为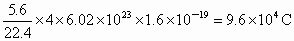 ,故B选项也正确.从原电池总反应可知放电一段时间后由于KOH→ ,故B选项也正确.从原电池总反应可知放电一段时间后由于KOH→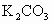 ,故溶液的碱性减弱,pH下降,故D不正确. ,故溶液的碱性减弱,pH下降,故D不正确. |

练习册系列答案
相关题目
 Pb + PbO2 + 2H2SO4
Pb + PbO2 + 2H2SO4 Pb + PbO2 + 2H2SO4
Pb + PbO2 + 2H2SO4