题目内容
氮化硅是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
______SiO2+______C+______N2 ______Si3N4+______CO
______Si3N4+______CO
(1)配平上述反应的化学方程式(将化学计量数填在方框内);
(2)该反应中的氧化剂是__________,其还原产物是_____________。
(3)该反应的平衡常数表达式为K=_______________________;
(4)将知上述反应为放热反应,则其反应热△H________零(填“大于”、“小于”或“等于”);升高温度,其平衡常数值________(填“增大”、“减小”或“不变”);
(5)若使压强增大,则上述平衡向_______反应方向移动(填“正”或“逆”);
(6)若已知CO生成速率为v (CO)=18mol/(L·min),则N2消耗速率为v (N2) =__________mol/(L·min)。
______SiO2+______C+______N2
 ______Si3N4+______CO
______Si3N4+______CO (1)配平上述反应的化学方程式(将化学计量数填在方框内);
(2)该反应中的氧化剂是__________,其还原产物是_____________。
(3)该反应的平衡常数表达式为K=_______________________;
(4)将知上述反应为放热反应,则其反应热△H________零(填“大于”、“小于”或“等于”);升高温度,其平衡常数值________(填“增大”、“减小”或“不变”);
(5)若使压强增大,则上述平衡向_______反应方向移动(填“正”或“逆”);
(6)若已知CO生成速率为v (CO)=18mol/(L·min),则N2消耗速率为v (N2) =__________mol/(L·min)。
(1)3,6,2,1,6
(2)N2;Si3N4
(3)K=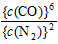
(4)小于;减小
(5)逆
(6)6
(2)N2;Si3N4
(3)K=
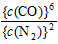
(4)小于;减小
(5)逆
(6)6

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案
相关题目
 氮化硅是一种新型陶瓷材料,它可由石英晶体与焦炭颗粒在高温的氮气流中,通过如下反应制得:3SiO2+6C+2N2
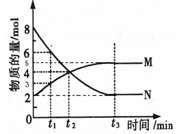
氮化硅是一种新型陶瓷材料,它可由石英晶体与焦炭颗粒在高温的氮气流中,通过如下反应制得:3SiO2+6C+2N2 Si3N4+6CO,该反应过程中的能量变化如图所示;回答下列问题:
Si3N4+6CO,该反应过程中的能量变化如图所示;回答下列问题: 氮化硅是一种新型陶瓷材料的主要成分,能承受高温,可用于制造业、航天业等领域.图是氮、硅的原子结构示意图,请推测氮化硅的化学式(分子式)为( )
氮化硅是一种新型陶瓷材料的主要成分,能承受高温,可用于制造业、航天业等领域.图是氮、硅的原子结构示意图,请推测氮化硅的化学式(分子式)为( ) 该反应过程中的能量变化如图所示,回答下列问题。
该反应过程中的能量变化如图所示,回答下列问题。 Si3N4 + 6CO,该反应过程中的能量变化如图所示;回答下列问题:
Si3N4 + 6CO,该反应过程中的能量变化如图所示;回答下列问题:
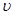 (正)
(正)