题目内容
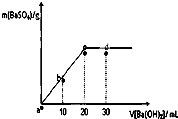 常温下,向0.25mol?L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中不正确的是( )
常温下,向0.25mol?L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中不正确的是( )| A、硫酸溶液的体积为20 mL |
| B、b时刻溶液中硫酸根离子浓度约为0.125 mol?L-1 |
| C、d时刻溶液的pH为13 |
| D、溶液的导电能力:c<d<b<a |
考点:离子方程式的有关计算
专题:计算题
分析:硫酸和氢氧化钡的反应方程式为H2SO4+Ba(OH)2=BaSO4↓+2H2O,随着氢氧化钡溶液的加入,溶液中氢离子的浓度逐渐降低,当达到c点时,硫酸和氢氧化钡恰好反应生成硫酸钡和水,继续滴加氢氧化钡溶液,氢氧化钡过量导致溶液成为氢氧化钡溶液.
A.根据恰好反应计算硫酸体积;
B.根据c=
计算硫酸根离子浓度;
C.先计算氢氧根离子浓度,根据水的离子积常数计算氢离子浓度,再求pH;
D.导电能力与溶液中自由移动离子的浓度有关,离子浓度越大,导电能力越强,随着氢氧化钡溶液的加入,溶液中硫酸根离子和氢离子逐渐减少,当达到c点时,硫酸和氢氧化钡恰好反应生成硫酸钡和水,溶液的导电性最小,继续滴加氢氧化钡溶液时,氢氧化钡是可溶性的强电解质,溶液中自由移动的离子浓度增大,导电性逐渐增强,所以导电能力是先减小后增大,但d中离子浓度小于b.
A.根据恰好反应计算硫酸体积;
B.根据c=
| n |
| V |
C.先计算氢氧根离子浓度,根据水的离子积常数计算氢离子浓度,再求pH;
D.导电能力与溶液中自由移动离子的浓度有关,离子浓度越大,导电能力越强,随着氢氧化钡溶液的加入,溶液中硫酸根离子和氢离子逐渐减少,当达到c点时,硫酸和氢氧化钡恰好反应生成硫酸钡和水,溶液的导电性最小,继续滴加氢氧化钡溶液时,氢氧化钡是可溶性的强电解质,溶液中自由移动的离子浓度增大,导电性逐渐增强,所以导电能力是先减小后增大,但d中离子浓度小于b.
解答:
解:A.硫酸和氢氧化钡的反应方程式为H2SO4+Ba(OH)2=BaSO4↓+2H2O,随着氢氧化钡溶液的加入,溶液中氢离子的浓度逐渐降低,溶液的PH值逐渐增大,当达到c点时,硫酸和氢氧化钡恰好反应生成硫酸钡和水,由于硫酸物质的量浓度和氢氧化钡溶液物质的量浓度相等,所以硫酸溶液的体积为20mL,故A正确;
B.b时刻硫酸根离子物质的量浓度为:
=0.167mol/L,故B错误;
C.d溶液呈碱性,c(OH-)=
=0.1mol/L,c(H+)=
=10-13,pH=13,故C正确;
D.导电能力与溶液中自由移动离子的浓度有关,离子浓度越大,导电能力越强,随着氢氧化钡溶液的加入,溶液中硫酸根离子和氢离子逐渐减少,当达到c点时,硫酸和氢氧化钡恰好反应生成硫酸钡和水,溶液的导电性最小,继续滴加氢氧化钡溶液时,氢氧化钡是可溶性的强电解质,溶液中自由移动的离子浓度增大,导电性逐渐增强,所以导电能力是先减小后增大,但d中离子浓度小于b,所以导电能力大小顺序是a>b>d>c,故D正确;
故选B.
B.b时刻硫酸根离子物质的量浓度为:
| 0.25mol/L×20mL |
| 20mL+10mL |
C.d溶液呈碱性,c(OH-)=
| 10mL×0.25mol/L×2 |
| 20mL+30mL |
| 1×10-14 |
| 0.1 |
D.导电能力与溶液中自由移动离子的浓度有关,离子浓度越大,导电能力越强,随着氢氧化钡溶液的加入,溶液中硫酸根离子和氢离子逐渐减少,当达到c点时,硫酸和氢氧化钡恰好反应生成硫酸钡和水,溶液的导电性最小,继续滴加氢氧化钡溶液时,氢氧化钡是可溶性的强电解质,溶液中自由移动的离子浓度增大,导电性逐渐增强,所以导电能力是先减小后增大,但d中离子浓度小于b,所以导电能力大小顺序是a>b>d>c,故D正确;
故选B.
点评:本题是图象解析题,难度较大,分析图象时要注意曲线的“原点”、“交点”、“转折点”等的意义,对“数”、“形”、“义”、“性”进行综合思考,从中发掘隐含信息快速解题.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
0.25L NaOH溶液中溶有10g NaOH,则此溶液的物质的量浓度为( )
| A、2 mo1/L |
| B、1 mo1/L |
| C、0.5 mo1/L |
| D、0.05 mo1/L |
某化学科研小组研究合成氨:N2(g)+3H2(g)═2NH3(g);△H<0,在其他条件不变时,改变某一条件时对化学平衡的影响,得到如下图象,以下对应选项中正确的是( )
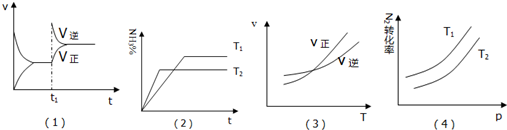

| A、(1)对应的是:在t1时恒压条件下,通入NH3 |
| B、(2)对应的是:氨气在恒容不同温度下的百分含量 |
| C、(3)对应的是:在恒容条件下,反应速率与温度的关系 |
| D、(4)对应的是:N2转化率与温度(T1>T2)、压强的关系 |
下列与化学反应能量变化相关的叙述正确的是( )
| A、生成物总能量一定低于反应物总能量 |
| B、等量H2在O2中完全燃烧,生成H2O(g)与生成H2O(l)放出的能量相同 |
| C、应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |
若NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、0℃、101 kPa时,22.4 L SO3所含的分子数为NA |
| B、标准状况下,22.4 L N2和O2的混合气体中含有的原子总数为2NA |
| C、0.1 mol Fe在0.1 mol Cl2中充分燃烧,转移的电子数为0.3NA |
| D、16 g CH4与18 g NH4+所含质子数均为10NA |
反应2A(g)?2B(s)+E(g)△H>0,在恒容容器中达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是( )
| A、移走部分A | B、减压 |
| C、增大E的浓度 | D、降温 |
下列有关实验操作的叙述正确的是( )
| A、为鉴别KCl、AlCl3和MgCl2溶液,分别向三种溶液中滴加NaOH溶液至过量 |
| B、进行焰色反应时,所用铂丝先用NaOH溶液洗涤并充分灼烧 |
| C、用托盘天平称取1.06 g无水碳酸钠,溶于250 mL水,配制0.04 mol?L-1 Na2CO3溶液 |
| D、为减小误差,配制溶液时容量瓶必须洗净并烘干后才能使用 |
 美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图:
美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图: