题目内容
11.工业上将Cl2通入KOH热溶液中制取KClO3(混有KClO).实验室模拟上述制备:向含18molKOH的溶液中通入Cl2,充分反应后测得溶液中n(Cl-)=12mol,将此溶液低温蒸干,所得到固体中KClO3的物质的量可能为( )| A. | 1.5mol | B. | 2.1mol | C. | 2.4 mol | D. | 3.0 mol |
分析 在氧化还原反应中转移电子数相等,且各元素的原子个数相等,假设反应后溶液中的溶质是氢氧化钾和氯酸钾结合得失电子守恒计算氯酸钾的物质的量,假设反应后溶液中的溶质是氯酸钾和次氯酸钾,根据钾离子守恒和得失电子守恒计算氯酸钾的物质的量.
解答 解:假设反应后溶液中的溶质是氢氧化钾和氯酸钾,根据转移电子守恒得氯酸钾的物质的量=$\frac{12mol×(1-0)}{5-0}$=2.4mol;
假设反应后溶液中的溶质是次氯酸钾和氯酸钾,
设氯酸钾的物质的量为x,次氯酸钾的物质的量为y,
根据转移电子守恒和钾离子守恒得方程式组$\left\{\begin{array}{l}{5x+y×1=12×1}\\{x+y+12=18}\end{array}\right.$,
所以得$\left\{\begin{array}{l}{x=1.5}\\{y=4.5}\end{array}\right.$,
实际上溶液中含有氯酸钾和次氯酸钾,所以得到的氯酸钾的物质的量可能为1.50mol,
故选A.
点评 本题考查了物质的量的有关计算,根据溶液中的溶质及转移电子守恒和钾原子守恒来分析解答即可,难度中等.

练习册系列答案
相关题目
6.下列有关烷烃的命名错误的是( )
| A. | 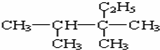 ,3,3-三甲基戊烷 ,3,3-三甲基戊烷 | B. | 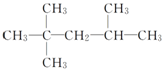 2,2,4三甲基戊烷 2,2,4三甲基戊烷 | ||
| C. | (CH3CH2)2CHCH3 3甲基戊烷 | D. | 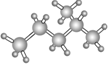 异戊烷 异戊烷 |
2.以下数值等于阿伏加德罗常数的是( )
| A. | 2.0g H218O与T2O的混合物中所含中子数 | |
| B. | 250mL 1mol/LFeCl3溶液中,阴、阳离子总数 | |
| C. | 标准状况下,7g某单烯烃A中的C-H键数 | |
| D. | 200mL 10mol/L盐酸与足量MnO2反应,转移电子数 |
19.为了保护环境,充分利用资源.某研究小组通过如图简化流程,将工业制硫酸的硫铁矿烧渣(主要以Fe2O3存在,还含有氧化铝、二氧化硅等杂质)转变成重要的化工原料FeSO4(反应条件略)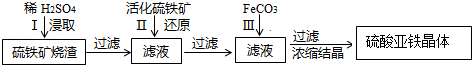
活化硫铁矿还原Fe3+的主要反应为:FeS2+7Fe2(S04)3+8H2O→15FeSO4+8H2SO4,不考虑其它反应,已知各氢氧化物沉淀PH值,请回答下列问题:
(1)第Ⅲ步目的是调剂PH,去除铝杂质(或除去Al(OH)3\Fe(OH)3).
(2)检验所得绿矾晶体中是否含有Fe3+的实验操作为取少量晶体溶于水,滴加KSCN溶液,若不出现血红色,(或滴加苯酚溶液,不出现紫色)表明不含有Fe3+,反之则含.
(3)得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质,②温度低、用水少降低洗涤过程中硫酸亚铁晶体的损耗.
研究性学习小组对硫酸亚铁晶体(FeSO4•xH2O)热分解研究,该小组同学称取ag硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行探究:
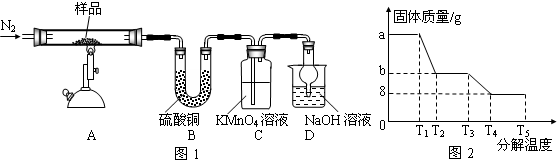
(4)装置B的目的是检验产物水生成;装置C中高锰酸钾溶液褪色,使之褪色的物质的名称是二氧化硫;装置D中球形干燥管的作用是防止氢氧化钠溶液倒吸.
(5)硫酸亚铁晶体完全分解后装置A中残留红棕色固体.写出FeSO4分解的化学方程式2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.
(6)设计一个简单实验检验产生的含硫元素的气体: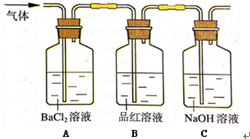 .
.
(7)某研究所利用SDTQ600热分析仪对硫酸亚铁晶体(FeSO4•xH2O)进行热分解,获得相关数据,绘制成固体质量--分解温度的关系如图2,由此得出FeSO4•xH2O中的x值为$\frac{10a-152}{18}$.

活化硫铁矿还原Fe3+的主要反应为:FeS2+7Fe2(S04)3+8H2O→15FeSO4+8H2SO4,不考虑其它反应,已知各氢氧化物沉淀PH值,请回答下列问题:
| pH | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 5.8 | 8.8 |
| Fe(OH)3 | 1.1 | 3.2 |
| Al(OH)3 | 3.0 | 5.0 |
(2)检验所得绿矾晶体中是否含有Fe3+的实验操作为取少量晶体溶于水,滴加KSCN溶液,若不出现血红色,(或滴加苯酚溶液,不出现紫色)表明不含有Fe3+,反之则含.
(3)得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质,②温度低、用水少降低洗涤过程中硫酸亚铁晶体的损耗.
研究性学习小组对硫酸亚铁晶体(FeSO4•xH2O)热分解研究,该小组同学称取ag硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行探究:

(4)装置B的目的是检验产物水生成;装置C中高锰酸钾溶液褪色,使之褪色的物质的名称是二氧化硫;装置D中球形干燥管的作用是防止氢氧化钠溶液倒吸.
(5)硫酸亚铁晶体完全分解后装置A中残留红棕色固体.写出FeSO4分解的化学方程式2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.
(6)设计一个简单实验检验产生的含硫元素的气体:
 .
.(7)某研究所利用SDTQ600热分析仪对硫酸亚铁晶体(FeSO4•xH2O)进行热分解,获得相关数据,绘制成固体质量--分解温度的关系如图2,由此得出FeSO4•xH2O中的x值为$\frac{10a-152}{18}$.
6.以环戊烷为原料制备环戊二烯的合成路线如图,则( )
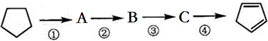

| A. | A的结构简式是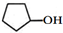 | |
| B. | ①②的反应类型分别是取代、消去 | |
| C. | 反应②③的条件分别是浓硫酸加热、光照 | |
| D. | 酸性KMnO4溶液褪色可证明 已完全转化 已完全转化 |
16.Na、Al、Fe都是重要的金属元素.下列说法正确的是( )
| A. | 三者的氧化物都是碱性氧化物 | |
| B. | 三者的氢氧化物都是白色固体 | |
| C. | 三者的氯化物都可用化合反应制得 | |
| D. | 三者的单质在空气中最终都生成氧化物 |
3.瑞香素具有消炎杀菌作用,结构如图所示,下列叙述正确的是( )
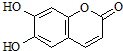

| A. | 与稀H2SO4混合加热不反应 | |
| B. | 不能使酸性高锰酸钾溶液褪色 | |
| C. | 1mol 瑞香素最多能与3mol Br2发生反应 | |
| D. | 1mol瑞香素与足量的NaOH溶液发生反应时,消耗NaOH 3mol |
20.离子方程式Ba2++2OH-+2H++SO42-→BaSO4↓+2H2O可表示( )
| A. | Ba(OH)2与NaHSO4两溶液的溶质按物质的量之比2:1反应 | |
| B. | Ba(OH)2与NaHSO4两溶液的溶质按物质的量之比1:2反应 | |
| C. | Ba(OH)2与NH4HSO4两溶液的溶质按物质的量之比2:1反应 | |
| D. | Ba(OH)2与NH4HSO4两溶液的溶质按物质的量之比1:2反应 |
1.PX是纺织工业的基础原料,其结构简式为 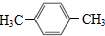 ,下列关于PX的说法正确的是( )
,下列关于PX的说法正确的是( )
 ,下列关于PX的说法正确的是( )
,下列关于PX的说法正确的是( )| A. | 属于饱和烃 | B. | 其一氯代物有四种 | ||
| C. | 可用于生产对苯二甲酸 | D. | 分子中所有原子都处于同一平面 |