题目内容
5.DDT又叫滴滴涕,化学名为双对氯苯基三氯乙烷,化学式(ClC6H4)2CH(CCl3).名称从英文缩写DDT而来,为白色晶体,不溶于水,溶于煤油,可制成乳剂,是有效的杀虫剂.DDT进入食物链,是导致一些食肉和食鱼的鸟接近灭绝的主要原因.因此从70年代后滴滴涕逐渐被世界各国明令禁止生产和使用,其结构为: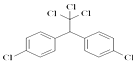 ,下列有关说法正确的是( )
,下列有关说法正确的是( )| A. | 属于烃类 | |
| B. | DDT完全燃烧后只产生CO2和H2O两种物质 | |
| C. | 分子无手性碳 | |
| D. | 核磁共振氢谱中显示有2组峰 |
分析 A.烃类物质只含有C、H两种元素;
B.根据元素守恒,还含有氯元素物质;
C.连接4个不同原子或原子团的碳原子为手性碳原子;
D.分子中含有3转化化学环境不同的H原子.
解答 解:A.烃类物质只含有C、H两种元素,而DDT中还含有氯原子,不属于烃类,故A错误;
B.根据元素守恒,还含有氯元素物质,故B错误;
C.连接4个不同原子或原子团的碳原子为手性碳原子,分子中没有手性碳原子,故C正确;
D.分子中含有3转化化学环境不同的H原子,氢核磁共振谱图中有3种位置峰,故D错误.
故选C.
点评 本题考查有机物的结构和性质,为高频考点,题目难度中等,注意有机物的空间结构同,结合官能团的性质解答该类题目.

练习册系列答案
相关题目
15.下列有关说法正确的是( )
| A. | 酸性溶液中不存在一水合氨分子 | |
| B. | 稀释pH=3的醋酸,溶液中所有离子浓度均降低 | |
| C. | 常温下,pH均为10的NaOH溶液和NaCN溶液中,由水电离出来的H+浓度相等 | |
| D. | 向氢氧化镁的悬浊液中加少量的水,平衡向溶解方向移动且c(Mg2+)不变 |
16.设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 30g甲醛和醋酸的混合物中含碳原子数目为nA | |
| B. | 22.4LCl2与足量的NaOH溶液反应,转移的电子数为2nA | |
| C. | 100mL0.2mol•L-1AlCl3溶液中,含Al3+数为0.02nA | |
| D. | 25℃,pH=13的NaOH溶液中,OH个数为0.1nA |
13.下列叙述与胶体知识无关的是( )
| A. | “卤水点豆腐” | |
| B. | 明矾可用作净水剂 | |
| C. | 在电影院看电影,会看到从放映室到银幕的光柱 | |
| D. | 向氯化铁溶液中加入过量氢氧化钠溶液会看到红褐色沉淀 |
20.下列说法正确的是( )
| A. | 苯的同系物都能使酸性高锰酸钾溶液褪色 | |
| B. | 红外光谱、核磁共振氢谱都可以鉴别乙醇和甲醚 | |
| C. | 符合相同通式的不同物质一定是同系物 | |
| D. | 某有机物燃烧后只生成二氧化碳和水,则一定不含有氧元素 |
10.下列醇中既能发生消去反应,又能被氧化为酮的是( )
①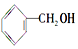
②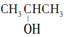
③CH3OH
④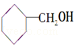
⑤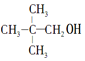
⑥
①

②
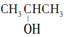
③CH3OH
④

⑤
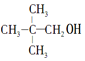
⑥

| A. | ①④⑤ | B. | ②④ | C. | ②⑥ | D. | ①②⑥ |
17.设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 将1 mol BaCl2 溶于水所形成的溶液中含NA个氯离子 | |
| B. | 2克氢气所含原子数约为6.02×1023 | |
| C. | 标准状况下,22.4 L SO2所含的分子数为NA | |
| D. | 常温常压下,22.4 L O2和O3的混合气体所含分子数为2NA |
14.下列物质溶于水能导电,但不属于电解质的是( )
| A. | 过氧化钠 | B. | 蔗糖 | C. | 氯气 | D. | 氯化铁 |
16.实验室常用氯化铵与氢氧化钙的固体混合加热制取氨气,实验室提供的有关装置见表:
完成下列填空:
(1)从图中选择实验室制取氨气的发生装置b(选填编号)、收集装置①(选填编号).
(2)用注射器收集50mL纯净的氨气,然后再抽取10mL滴有酚酞试液的蒸馏水,并用橡皮塞封闭针头.充分振荡后注射器内无(选填“有”“无”)气体剩余,液体呈红色,用化学方程式解释液体颜色变化的原因NH3+H2O?NH3•H2O?NH4++OH-.
(3)工业合成氨的简易流程如图:
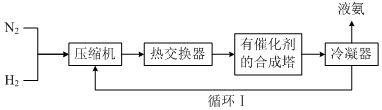
通过循环Ⅰ可利用的气态物质是d
a.催化剂 b.只有N2c.只有H2 d.N2和H2
(4)将 CO2通入到氨化的饱和食盐水中制备NaHCO3固体,反应的化学方程式NaCl+CO2+NH3+H2O→NaHCO3↓+NH4Cl.29NH3、PH3、
AsH3三种氢化物热稳定性由强到弱的顺序是NH3>PH3>AsH3,理由是N、P、As原子半径依次增大,使得N-H、P-H、As-H键长依次增长,热稳定性逐渐减弱.
(5)工业上用氨水吸收SO2尾气,最终得到化肥 (NH4)2SO4.(NH4)2SO4溶液呈酸性,用离子方程式解释原因NH4++H2O=NH3•H2O+H+;该溶液中存在多种守恒,用离子浓度表示其中一种守恒关系电荷守恒为:[NH4+]+[H+]=2[SO42-]+[OH-]或者物料守恒为:2[SO42-]=[NH4+]+[NH3•H2O].
| 气体发生装置 | 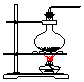 a | 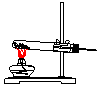 b |  c |
| 气体收集装置 | 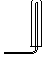 2 | 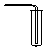 ② | 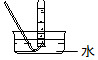 ③ |
(1)从图中选择实验室制取氨气的发生装置b(选填编号)、收集装置①(选填编号).
(2)用注射器收集50mL纯净的氨气,然后再抽取10mL滴有酚酞试液的蒸馏水,并用橡皮塞封闭针头.充分振荡后注射器内无(选填“有”“无”)气体剩余,液体呈红色,用化学方程式解释液体颜色变化的原因NH3+H2O?NH3•H2O?NH4++OH-.
(3)工业合成氨的简易流程如图:

通过循环Ⅰ可利用的气态物质是d
a.催化剂 b.只有N2c.只有H2 d.N2和H2
(4)将 CO2通入到氨化的饱和食盐水中制备NaHCO3固体,反应的化学方程式NaCl+CO2+NH3+H2O→NaHCO3↓+NH4Cl.29NH3、PH3、
AsH3三种氢化物热稳定性由强到弱的顺序是NH3>PH3>AsH3,理由是N、P、As原子半径依次增大,使得N-H、P-H、As-H键长依次增长,热稳定性逐渐减弱.
(5)工业上用氨水吸收SO2尾气,最终得到化肥 (NH4)2SO4.(NH4)2SO4溶液呈酸性,用离子方程式解释原因NH4++H2O=NH3•H2O+H+;该溶液中存在多种守恒,用离子浓度表示其中一种守恒关系电荷守恒为:[NH4+]+[H+]=2[SO42-]+[OH-]或者物料守恒为:2[SO42-]=[NH4+]+[NH3•H2O].