题目内容
11.汽油中某成分X的分子式为C6H14,其一氯代物有4种可能的结构,则X的结构简式为( )| A. |  | B. |  | C. |  | D. |  |
分析 X的分子式为C6H14,通式判断为烷烃,其一氯代物有4种可能的结构,说明结构中含四种不同氢原子,据此分析选项;
解答 解:A. 分子中含5种氢原子,一氯代物5种,故A错误;
分子中含5种氢原子,一氯代物5种,故A错误;
B. 分子中含四种氢原子,其一氯代物有4种可能的结构,故B正确;
分子中含四种氢原子,其一氯代物有4种可能的结构,故B正确;
C. 分子中含两种氢原子,其一氯代物有2种可能的结构,故C错误;
分子中含两种氢原子,其一氯代物有2种可能的结构,故C错误;
D. 分子中含三种氢原子,其一氯代物有3种可能的结构,故D错误;
分子中含三种氢原子,其一氯代物有3种可能的结构,故D错误;
故选B.
点评 本题考查了同分异构体中氢原子种类的分析判断、分子中含多少不同氢原子,其一氯代物种类有多少,题目难度中等.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
4.关于 的分子结构说法正确的是( )
的分子结构说法正确的是( )
 的分子结构说法正确的是( )
的分子结构说法正确的是( )| A. | 分子中12个碳原子一定在同一平面 | |
| B. | 分子中有7个碳原子可能在同一直线上 | |
| C. | 分子中最多有6个碳原子能在同一直线上 | |
| D. | 分子中最多有8个碳原子能在同一直线上 |
4. 已知碳碳单键可以绕键轴自由旋转,苯环为平面结构,现在有一种结构简式为如图所示的烃,下列说法中正确的是( )
已知碳碳单键可以绕键轴自由旋转,苯环为平面结构,现在有一种结构简式为如图所示的烃,下列说法中正确的是( )
 已知碳碳单键可以绕键轴自由旋转,苯环为平面结构,现在有一种结构简式为如图所示的烃,下列说法中正确的是( )
已知碳碳单键可以绕键轴自由旋转,苯环为平面结构,现在有一种结构简式为如图所示的烃,下列说法中正确的是( )| A. | 分子中至少有9个碳原子处于同一平面上 | |
| B. | 分子中至少有10个碳原子处于同一平面上 | |
| C. | 分子中至少有11个碳原子处于同一平面上 | |
| D. | 分子中至少有16个碳原子处于同一平面上 |
1.下列实验能获得成功的是( )
| A. | 苯、溴水、铁粉混合制成溴苯 | |
| B. | 加浓溴水,然后过滤可除去苯中少量苯酚 | |
| C. | 用高锰酸钾酸性溶液来区别甲烷和乙烯 | |
| D. | 可用分液漏斗分离乙醇和水 |
3.下列分子中所有原子不可能共平面的是( )
| A. |  | B. | CF2═CF2 | C. | CH≡C-CH═CH2 | D. |  |
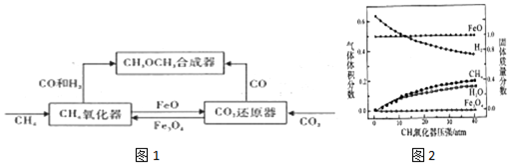
1.一种通过铁基氧载体(Fe3O4/FeO)深度还原和再生来合成二甲醚(CH3OCH3)的原理如图1:
(1)二甲醚的合成反应:3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)△H1
①已知CO、H2与CH3OCH的燃烧热(△H)分别为a kJ•mol-1、b kJ•mol-1、c kJ•mol-1、(a、b、c均小于0),则△H1=(3a+3b-c)kJ•mol-1.
②该反应选用CuO/ZnO/Al2O3复合催化剂,该催化剂能B、C(填标号).
A.促进平衡正向移动 B.提高反应速率
C.降低反应的活化能 D.改变反应的焓变
(2)CH4氧化器中发生的主反应:
ⅰ.CH4(g)+Fe3O4(s)?CO(g)+2H2(g)+3Fe(s)
ⅱ.CH4(g)+4Fe3O4(s)?CO2(g)+2H2O(g)+12FeO(s)
850℃时,压强和部分气体体积分数、固相各组分质量分数的关系如图2.
①随着压强的增大,反应ⅰ的平衡常数K值不变 (填“增大”、“减小”、或“不变”)
②结合图象,分析H2O的体积分数变化的原因Fe3O4+H2$\frac{\underline{\;高温\;}}{\;}$3FeO+H2O(用化学方程式表示)
(3)将一定量的FeO和CO2置于CO2还原器(体积不变的密闭容器)中,发生的主反应:
CO2(g)+3FeO(s)?Fe3O4(s)+CO (g)△H2
保持其他条件不变,测得不同温度下最终反应体系中CO、CO2体积分数如表:
①△H2< 0(填“>”或“<”).
②若在150℃时进行上述转化,理论转化率ɑ(FeO)=100%.
③在上述反应体系中,一定可以说明该反应达到平衡状态的是B、C、D(填标号).
A.体系的压强不变 B.CO2的物质的量不变
C.CO的生成速率和消耗速率相等且不等于零 D.气体的平均摩尔质量不变
④根据化学反应原理,分析CO2还原器温度设置在170℃的原因温度过高,CO2的转化率低;温度过低,反应速率比较慢.

(1)二甲醚的合成反应:3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)△H1
①已知CO、H2与CH3OCH的燃烧热(△H)分别为a kJ•mol-1、b kJ•mol-1、c kJ•mol-1、(a、b、c均小于0),则△H1=(3a+3b-c)kJ•mol-1.
②该反应选用CuO/ZnO/Al2O3复合催化剂,该催化剂能B、C(填标号).
A.促进平衡正向移动 B.提高反应速率
C.降低反应的活化能 D.改变反应的焓变
(2)CH4氧化器中发生的主反应:
ⅰ.CH4(g)+Fe3O4(s)?CO(g)+2H2(g)+3Fe(s)
ⅱ.CH4(g)+4Fe3O4(s)?CO2(g)+2H2O(g)+12FeO(s)
850℃时,压强和部分气体体积分数、固相各组分质量分数的关系如图2.
①随着压强的增大,反应ⅰ的平衡常数K值不变 (填“增大”、“减小”、或“不变”)
②结合图象,分析H2O的体积分数变化的原因Fe3O4+H2$\frac{\underline{\;高温\;}}{\;}$3FeO+H2O(用化学方程式表示)
(3)将一定量的FeO和CO2置于CO2还原器(体积不变的密闭容器)中,发生的主反应:
CO2(g)+3FeO(s)?Fe3O4(s)+CO (g)△H2
保持其他条件不变,测得不同温度下最终反应体系中CO、CO2体积分数如表:
| 温度I/℃ | 100 | 170 | 200 | 300 | 400 | 500 |
| CO2体积分数 | 0.67 | 0.67 | 0.75 | 0.82 | 0.9 | 0.92 |
| CO体积分数 | 0.33 | 0.33 | 0.25 | 0.18 | 0.1 | 0.08 |
②若在150℃时进行上述转化,理论转化率ɑ(FeO)=100%.
③在上述反应体系中,一定可以说明该反应达到平衡状态的是B、C、D(填标号).
A.体系的压强不变 B.CO2的物质的量不变
C.CO的生成速率和消耗速率相等且不等于零 D.气体的平均摩尔质量不变
④根据化学反应原理,分析CO2还原器温度设置在170℃的原因温度过高,CO2的转化率低;温度过低,反应速率比较慢.
 X
X Z.
Z.