题目内容
5.合成气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,通过反应进行甲醇合成,T1℃下此反应的平衡常数为160.此温度下,在密闭容器中加入一定量CO和H2,反应到某时刻测得各组分的浓度见下表.| 物质 | H2 | CO | CH3OH |
| 浓度/mol•L-1 | 0.2 | 0.1 | 0.4 |
②若其他条件不变,在T2℃反应10min后达到平衡,c(H2)=0.4mol•L-1,则该时间内反应速率v(CH3OH)=0.03mol/(L•min).
分析 ①计算此时的浓度商Qc,与平衡常数比较,判断反应进行的方向,据此解答;
②依据图表数据计算起始量,结合三段式列式计算,根据甲氢气的浓度变化计算甲醇的浓度变化量,再根据v=$\frac{△C}{△t}$计算v(CH3OH).
解答 解:①由表中数据可知,10min时氢气的浓度为0.2mol/L、CO的浓度为0.1mol/L、甲醇的浓度为0.4mol/L,则此时的浓度商Qc=$\frac{0.4}{0.{2}^{2}×0.1}$=100,小于平衡常数160,故反应向正反应方向进行,故V正>V逆,故答案为:>;
②依据图表可知和H2和CO的起始物质的量浓度分别为1mol/L和0.5mol/L.
2H2(g)+CO(g)?CH3OH(g)
起始量(mol/L) 1 0.5 0
变化量(mol/L) 0.8 0.4 0.4
T4时(mol/L) 0.2 0.1 0.4
若T1℃反应10min达到平衡,c(H2)=0.4mol•L-1,由表中数据可知,l0min内氢气的浓度变化量为0.6mol/L,故甲醇的浓度变化量为0.3mol/L,故v(CH3OH)=$\frac{0.3mol/L}{10min}$=0.03mol/(L•min),
故答案为:0.03mol/(L•min).
点评 本题考查了化学平衡的有关计算、化学平衡常数及应用等,难度不大,注意掌握平衡常数应用.

练习册系列答案
相关题目
15.下列各组的离子中,能在溶液中大量共存的是( )
| A. | K+、H+、SO42-、OH- | B. | Na+、H+、Cl-、CO32- | ||
| C. | Na+、Ca2+、CO32-、NO3- | D. | K+、Cu2+、Cl-、SO42- |
20.化学与生活密切相关.下列应用中利用了物质氧化性的是( )
| A. | 明矾-净化水 | B. | 漂白粉-漂白织物 | C. | 食醋-除水垢 | D. | 纯碱-去油污 |
10.下列说法正确的是( )
| A. | 1mol/L的NaCl溶液是指此溶液中含有1 mol NaCl | |
| B. | 从1L 0.5mo1/L的NaCl溶液中取出100 mL溶液,其物质的量浓度变为0.1mol/L | |
| C. | 0℃时,1molC12的体积约为22.4L | |
| D. | 1mol/L的CaCl2溶液中,Cl-的物质的量浓度为2mol/L |
8.下列有关物质应用的说法不正确的是( )
| A. | 铁制容器可盛装冷的浓硫酸,因为常温下铁和浓硫酸不反应 | |
| B. | Na2O2用作呼吸面具的供氧剂 | |
| C. | 欲鉴别FeCl2溶液、AlCl3溶液和AgNO3溶液,向3种待测液中分别滴加足量氨水 | |
| D. | 铝热反应需提供一定的能量引发,因为铝热反应为吸热反应 |
9.青霉素是医学上一种常用的抗生素,它在人体内经酸性水解后,得到青霉氨基酸,其结构简式为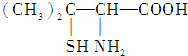
(分子中的-SH与-OH具有类似性质).下列关于青霉氨基酸的推断合理的是( )
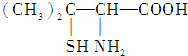
(分子中的-SH与-OH具有类似性质).下列关于青霉氨基酸的推断合理的是( )
| A. | 青霉氨基酸分子中所有碳原子均在同一直线上 | |
| B. | 青霉氨基酸具有两性并能发生酯化反应 | |
| C. | 青霉氨基酸分子间不能发生缩合反应 | |
| D. | 1 mol青霉氨基酸与足量的金属钠反应生成0.5 mol H2 |
 ,E元素的电子排布式为1s22s22p63s23p63d5s4s1.
,E元素的电子排布式为1s22s22p63s23p63d5s4s1.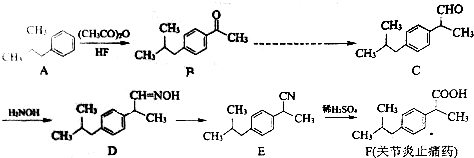
 .
.