题目内容
(10分)有A、B、C、D四种离子化合物,组成它们的离子分别为:
阳离子:Na+、Al3+、NH4+; 阴离子:OH-、NO3-、CO32-、HSO4-
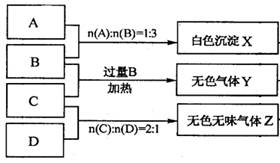
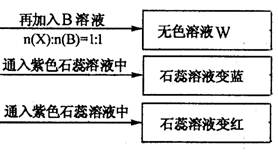
为鉴别四种化合物,某学生分别取少量固体配成溶液,编号为A、B、C、D进行实验。实验过程和记录如下图所示(无关物质已略去)
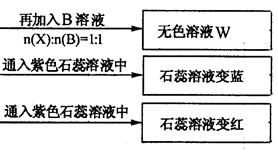
(1) Y、Z的化学式分别为:Y ;Z
(2)写出指定反应的离子方程式:
①加热条件下,C与过量B反应:
②D溶液显弱碱性的原因是(用离子方程式表示)
(3)等物质的量浓度的A、B、C、D溶液pH由大到小的顺序是(用化学式表示)
(4)若B、C的稀溶液混合后(不加热)溶液呈中性,则溶液中离子浓度从大到小的顺序是:
(1)NH3(1分) CO2(1分)
(2)①NH4++H++2OH-=NH3↑+2H2O(2分) ②CO32-+H2O HCO3-+OH- (2分)
HCO3-+OH- (2分)
(3) NaOH>Na2CO3>Al(NO3)3>NH4HSO4(2分)
(4) c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-)(2分)
解析

练习册系列答案
相关题目