题目内容
固体氧化物燃料电池(SOFC)以固体氧化物作为电解质介质,其工作原理如图所示.
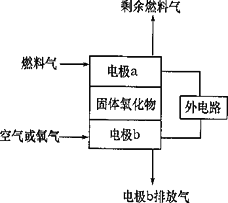
(1)电极b的电极反应式是________
(2)假设外电路是电解硫酸铜溶液的装置.若以C2H4为燃料气,工作一段时间后燃料电池中消耗了标准状况下的2.24 L C2H4,则外电路阴极区的产物及其物质的量分别是________ ________.
答案:
解析:
解析:
|
(1)O2+4e-→2O2-(2分) (2)Cu 0.6 mol(2分) |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
美国科学家成功开发便携式固体氧化物燃料电池,它以丙烷气体为燃料,每填充一次燃料,大约可连续24小时输出50W的电力.一极通入空气,另一极通入丙烷气体,电解质是固态氧化物,在熔融状态下能传导O2-,下列对该燃料电池的说法不正确的是( )
| A、在熔融电解质中,O2-由负极移向正极 | B、该电池的总反应是:C3H8+5O2→3CO2+4H2O | C、电路中每流过10 mol电子,标准状况下约有11.2 L丙烷被完全氧化 | D、通丙烷的电极为电池负极,发生的电极反应为:C3H8-20e-+10O2-=3CO2+4H2O |
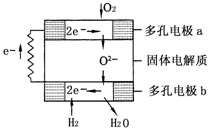 固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的.它以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的.它以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( ) CO(g)+H2(g)△H=+131.3kJ?mol-1,
CO(g)+H2(g)△H=+131.3kJ?mol-1,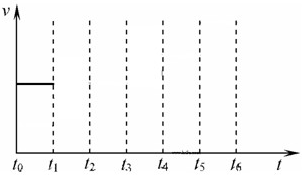 在一体积不变的容器中,当合成氨反应达到平衡后,在t1时升高温度,t2重新达到平衡,t3时充入氮气,t4时重新达到平衡,t5时移去一部分产物,t6时又达到平衡,请在下面的反应速率与时间关系图中画出t1到t5逆反应速率、t5到t6正反应速率的变化情况.
在一体积不变的容器中,当合成氨反应达到平衡后,在t1时升高温度,t2重新达到平衡,t3时充入氮气,t4时重新达到平衡,t5时移去一部分产物,t6时又达到平衡,请在下面的反应速率与时间关系图中画出t1到t5逆反应速率、t5到t6正反应速率的变化情况.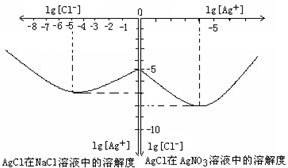
 如图所示是一种新近开发的固体氧化物燃料电池.它以掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体为固体电解质,在熔融状态下传导氧离子(O2-),其中多孔电极a、b均不参与电极反应.下列判断不正确的是( )
如图所示是一种新近开发的固体氧化物燃料电池.它以掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体为固体电解质,在熔融状态下传导氧离子(O2-),其中多孔电极a、b均不参与电极反应.下列判断不正确的是( )