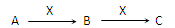��Ŀ����
 ����3�ֻ�����A��B��C����������Ԫ��R����ת����ϵ��ͼ��ʾ��
����3�ֻ�����A��B��C����������Ԫ��R����ת����ϵ��ͼ��ʾ��
��1����A�ɵ�������2��Ԫ����ɣ������£�0.1mol/L X��Һ��pH=13����A����
�ڱ��е�λ����______��X�������ӵĵ���ʽ��______��Bת��ΪC�����ӷ���ʽ��______��
��2����������A��B��C��X��Ϊ��̬���ʣ�1mol A�к��й��ۼ�����ĿԼΪ1.806��1024��XΪ���ʣ�A��X��Ӧ����B�Ļ�ѧ����ʽ��______����һ�������£�A����C��Ӧ����C�Դ�������Ⱦ���÷�Ӧ�Ļ�ѧ����ʽ��______��
�⣺��1�������£�0.1mol/L X��Һ��pH=13��XӦΪǿ�ΪNaOH��A�ɵ�������2��Ԫ����ɣ���������NaOH��Ӧ����BӦΪAl��OH��3��AΪAlCl3��CΪNaAlO2��Alλ��Ԫ�����ڱ��������ڢ�A�壬OH-���ӵĵ���ʽΪ ��Bת��ΪC�����ӷ���ʽ��Al��OH��3+OH-=AlO2-+2H2O��
��Bת��ΪC�����ӷ���ʽ��Al��OH��3+OH-=AlO2-+2H2O��
�ʴ�Ϊ���������ڢ�A�壻 ��Al��OH��3+OH-=AlO2-+2H2O��
��Al��OH��3+OH-=AlO2-+2H2O��
��2��������A��B��C��X��Ϊ��̬���ʣ�1molA�к��й��ۼ�����ĿԼΪ1.806��1024��ӦΪNH3��XΪ���ʣ�ӦΪO2��BΪNO��CΪNO2��
A��X��Ӧ����B�Ļ�ѧ����ʽ��4NH3+5O2 4NO+6H2O��
4NO+6H2O��
��һ�������£�A����C��Ӧ����C�Դ�������Ⱦ���÷�Ӧ�Ļ�ѧ����ʽ��8NH3+6NO2=7N2+12H2O��
�ʴ�Ϊ��4NH3+5O2 4NO+6H2O��8NH3+6NO2=7N2+12H2O��
4NO+6H2O��8NH3+6NO2=7N2+12H2O��
��������1�������£�0.1mol/L X��Һ��pH=13��XӦΪǿ�ΪNaOH��A�ɵ�������2��Ԫ����ɣ���������NaOH��Ӧ����BӦΪAl��OH��3��AΪAlCl3��CΪNaAlO2��
��2��������A��B��C��X��Ϊ��̬���ʣ�1molA�к��й��ۼ�����ĿԼΪ1.806��1024��ӦΪNH3��XΪ���ʣ�ӦΪO2��BΪNO��CΪNO2��
���������⿼��������ƶϣ���Ŀ�ѶȲ���ע����������Ϣ������ת����ϵ�жϷ�Ӧ���ص㣬������ʵĹ��ɺ������ƶ����ʵ����࣮
 ��Bת��ΪC�����ӷ���ʽ��Al��OH��3+OH-=AlO2-+2H2O��
��Bת��ΪC�����ӷ���ʽ��Al��OH��3+OH-=AlO2-+2H2O���ʴ�Ϊ���������ڢ�A�壻
 ��Al��OH��3+OH-=AlO2-+2H2O��
��Al��OH��3+OH-=AlO2-+2H2O����2��������A��B��C��X��Ϊ��̬���ʣ�1molA�к��й��ۼ�����ĿԼΪ1.806��1024��ӦΪNH3��XΪ���ʣ�ӦΪO2��BΪNO��CΪNO2��
A��X��Ӧ����B�Ļ�ѧ����ʽ��4NH3+5O2
 4NO+6H2O��
4NO+6H2O����һ�������£�A����C��Ӧ����C�Դ�������Ⱦ���÷�Ӧ�Ļ�ѧ����ʽ��8NH3+6NO2=7N2+12H2O��
�ʴ�Ϊ��4NH3+5O2
 4NO+6H2O��8NH3+6NO2=7N2+12H2O��
4NO+6H2O��8NH3+6NO2=7N2+12H2O����������1�������£�0.1mol/L X��Һ��pH=13��XӦΪǿ�ΪNaOH��A�ɵ�������2��Ԫ����ɣ���������NaOH��Ӧ����BӦΪAl��OH��3��AΪAlCl3��CΪNaAlO2��
��2��������A��B��C��X��Ϊ��̬���ʣ�1molA�к��й��ۼ�����ĿԼΪ1.806��1024��ӦΪNH3��XΪ���ʣ�ӦΪO2��BΪNO��CΪNO2��
���������⿼��������ƶϣ���Ŀ�ѶȲ���ע����������Ϣ������ת����ϵ�жϷ�Ӧ���ص㣬������ʵĹ��ɺ������ƶ����ʵ����࣮

��ϰ��ϵ�д�
�����Ŀ
 ����3�ֻ�����A��B��C����������Ԫ��R����ת����ϵ��ͼ��ʾ��
����3�ֻ�����A��B��C����������Ԫ��R����ת����ϵ��ͼ��ʾ��
 A��B��C����������Ԫ��R����ת����ϵ����ͼ��ʾ��
A��B��C����������Ԫ��R����ת����ϵ����ͼ��ʾ��