题目内容
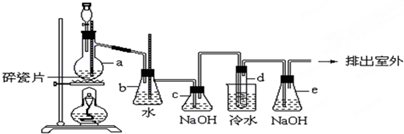
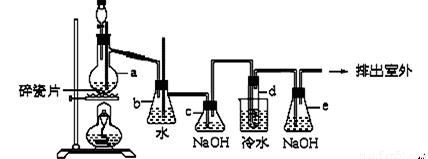
在实验中可以用KMnO4代替MnO2制Cl2,反应方程式为:2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O。
现有MnO2和KMnO4的混合物245 g,与足量的浓盐酸反应后得到的Cl2的质量为248.5 g,求原混合物中MnO2和KMnO4各多少克?
答案:
解析:
提示:
解析:
| 混合物中含MnO2 87 g,含KMnO4 158 g。
|
提示:
| 设混合物中MnO2的质量为x,KmnO4的质量为y:
MnO2+4HCl(浓) 87 71 x
2KMnO4+16HCl=== 2KCl+2MnCl2+5Cl2↑+8H2O 316 355 y
解得
|

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目