题目内容
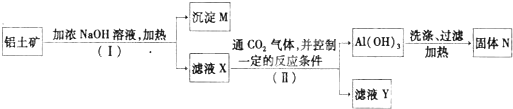
工业上用铝土矿(主要成分是Al2O3·H2O、Al2O3·3H2O以及少量Fe2O3、SiO2等)提取纯Al2O3作冶炼铝的原料。提取的操作过程可用以下流程图表示:
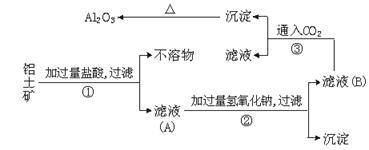
(1)写出滤液A中一种溶质与过量NaOH溶液反应进入滤液B中的离子方程式:_____________。
(2)若步骤①中没有过滤操作而直接进入步骤②,对后面操作将产生的影响是_______________。
(1)Al3++4OH-=[Al(OH)4]- (2)①中的不溶物(Na2SiO3)在操作②中会被氢氧化钠溶液溶解,最后所得Al2O3中将含有SiO2。
解析:
Al2O3为两性氧化物,能溶于盐酸和氢氧化钠;Fe2O3为碱性氧化物,溶于盐酸而不溶于氢氧化钠;SiO2为酸性氧化物,溶于氢氧化钠而不溶于盐酸.解答此题,关键要抓住这些氧化物性质的差异,形成分离、除杂质的思路。

练习册系列答案
相关题目