题目内容
化学与工农业生产、环境保护、日常生活等方面有广泛联系,下列叙述正确的是( )
| A、纯净水几乎不含任何杂质,喝纯净水比喝矿泉水对人体更有营养 |
| B、二氧化硫的大量排放是造成光化学烟雾的主要原因 |
| C、某雨水样品放置一段时间后,pH由4.68变为4.28,是因为雨水在放置过程中溶解了较多的CO2 |
| D、“84”消毒液的有效成分为NaClO,能杀菌消毒 |
考点:常见的生活环境的污染及治理
专题:化学应用
分析:A.纯净水加工时,在去除水中的污染物的同时也去除了水中人体必需的微量元素和宏量元素,经常喝纯净水会导致人体缺乏人体需要的无机盐以及一些微量元素;
B.光化学烟雾由碳氢化合物和氮氧化合物在阳光的作用下起化学反应所产生;
C.酸雨中亚硫酸为弱电解质,具有还原性,能被氧化成强电解质硫酸,溶液的PH减小;
D.“84”消毒液的有效成分为NaClO,NaClO的水溶液为无色液体,具有强氧化性;
B.光化学烟雾由碳氢化合物和氮氧化合物在阳光的作用下起化学反应所产生;
C.酸雨中亚硫酸为弱电解质,具有还原性,能被氧化成强电解质硫酸,溶液的PH减小;
D.“84”消毒液的有效成分为NaClO,NaClO的水溶液为无色液体,具有强氧化性;
解答:
解:A.纯净水不含人体所需的无机盐,应多喝矿泉水或自来水来补充,故A错误;
B.大气中碳氢化合物和氮氧化合物在阳光的作用下起化学反应所产生的化学污染物,故B错误;
C.饱和CO2溶液的PH等于5.6,而雨水的pHpH由4.68变为4.28,是由于2H2SO3+O2═2H2SO4,溶液的酸性增强,PH减小;故C错误;
D.“84”消毒液的有效成分为NaClO,具有强氧化性,可用于杀菌消毒,具有漂白性,可漂白浅色衣服,故D正确;
故选D.
B.大气中碳氢化合物和氮氧化合物在阳光的作用下起化学反应所产生的化学污染物,故B错误;
C.饱和CO2溶液的PH等于5.6,而雨水的pHpH由4.68变为4.28,是由于2H2SO3+O2═2H2SO4,溶液的酸性增强,PH减小;故C错误;
D.“84”消毒液的有效成分为NaClO,具有强氧化性,可用于杀菌消毒,具有漂白性,可漂白浅色衣服,故D正确;
故选D.
点评:本题考查纯净水、酸雨、光化学污染、“84”消毒液的有效成分等问题,题目难度不大,注意酸雨成分的化学性质以及光化学烟雾等问题.

练习册系列答案
相关题目
4一甲基一2一乙基一1一戊烯经催化加氢后所得产物的名称为( )
| A、4一甲基一2一乙基戊烷 |
| B、2,5一二甲基戊烷 |
| C、2一乙基一4一甲基戊烷 |
| D、2,4一二甲基己烷 |
下列说法中不正确的是( )
| A、可燃物遇到氧气不一定燃烧 |
| B、缓慢氧化不一定能引起自燃 |
| C、自燃不一定由缓慢氧化引起 |
| D、剧烈燃烧不一定引起爆炸 |
与SO3互为等电子体的分子是( )
| A、H3O+ |
| B、SO32- |
| C、NH3 |
| D、CO32- |
下列化学用语正确的是( )
A、H2O2的电子式: | ||
B、丙烷分子的球棍模型: | ||
C、CO2的比例模型: | ||
D、原子核内有20个中子的氯原子:
|
下列说法正确的是( )
| A、利用SO2的漂白性可使酸性高锰酸钾溶液褪色 |
| B、漂白粉既可做漂白棉麻纸张的漂白剂,又可做游泳池及环境的消毒剂 |
| C、为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质 |
| D、为增强漂白效果,可将等物质的量的SO2和Cl2混合使用以达到增强效果的目的 |
设NA为阿伏加德罗常数的数值,则下列说法正确的是( )
| A、2.24 L C4H6中含有碳碳叁键数一定为0.1×6.02×1023 |
| B、在标准状态下,11.2L NO与11.2L O2混合后气体分子数为0.75NA |
| C、106g Na2CO3固体中的阴离子数为NA |
| D、含1molFeCl3的饱和溶液滴入沸水中得到氢氧化铁胶体粒子数目为NA |
 某两种物质在一定条件下能发生化学反应,其反应的微观示意图如图,则下列说法中,正确的是(说明:一种小球代表一种元素的原子)( )
某两种物质在一定条件下能发生化学反应,其反应的微观示意图如图,则下列说法中,正确的是(说明:一种小球代表一种元素的原子)( )| A、图中的反应物都是化合物 |
| B、该反应属于置换反应 |
| C、该反应属于复分解反应 |
| D、该反应不符合质量守恒定律 |
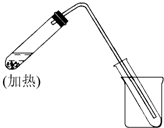 如图是用自来水制取少量蒸馏水的简易装置(加热及固定仪器略),其原理与教材中的实验完全相同.回答下列问题:
如图是用自来水制取少量蒸馏水的简易装置(加热及固定仪器略),其原理与教材中的实验完全相同.回答下列问题: