题目内容
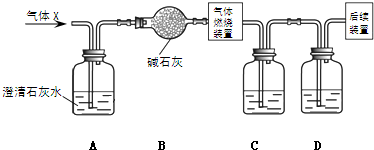
某无色气体X,可能含有CO2、SO2、HCl、HBr中的一种或几种.将X通过适量的氯水时,X恰好完全反应,没有任何气体剩余.将所得的无色溶液分装于两支试管后,分别加入酸化的AgNO3与BaCl2溶液,结果均产生白色沉淀.下列推论正确的是( )
| A.X中一定没有CO2 |
| B.X中一定有SO2,产生的沉淀是AgCl与BaSO4 |
| C.X中一定没有HBr |
| D.X中一定有HCl |
将X通过适量的氯水时,X恰好完全反应,没有任何气体剩余,能与氯气反应的有SO2、HBr,说明一定无CO2、HCl.加入酸化的BaCl2溶液,结果产生白色沉淀,说明一定有SO2,沉淀为硫酸钡;加入酸化的AgNO3溶液,产生白色沉淀为氯化银,但氯水中含有氯元素,不能确定原气体含氯化氢.
故选AB.
故选AB.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目


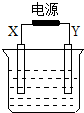 如图,X和Y均为石墨电极:
如图,X和Y均为石墨电极: