题目内容
下列物质中能证明某化合物中一定有离子键的是( )
| A、晶体可溶于水 |
| B、具有较高的熔点 |
| C、水溶液可导电 |
| D、熔融状态能导电 |
考点:离子化合物的结构特征与性质
专题:
分析:离子化合物具有较高的熔点,含有离子键,在熔融状态下或水溶液中能导电,但共价化合物在水溶液中也能导电.
解答:
解:A.离子化合物和共价化合物都能溶于水,与化学键类型没有关系,故A错误;
B.具有较高熔点的物质不一定含有离子键,可能只含共价键,如金刚石等,故B错误;
C.水溶液可导电的不一定含有离子键,如氨气,故C错误;
D.熔融状态下能导电的化合物,该化合物在熔融状态下电离出自由移动的阴阳离子而导电,所以一定含有离子键,故D正确;
故选D.
B.具有较高熔点的物质不一定含有离子键,可能只含共价键,如金刚石等,故B错误;
C.水溶液可导电的不一定含有离子键,如氨气,故C错误;
D.熔融状态下能导电的化合物,该化合物在熔融状态下电离出自由移动的阴阳离子而导电,所以一定含有离子键,故D正确;
故选D.
点评:本题考查离子键的判断,侧重考查基本概念,明确离子键和共价键的区别是解本题关键,注意化学键与物质的溶解性无关,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组物质互为同系物的是( )
| A、甲醇与乙醇 |
B、 与 与 |
| C、二甲苯与乙苯 |
| D、2,2-二甲基丙烷与新戊烷 |
下列反应中生成物总能量高于反应物总能量的是( )
| A、纯碱水解反应 |
| B、乙醇燃烧 |
| C、铝热反应 |
| D、氧化钙溶于水 |
2004年4月30号出版的《Science》杂志报道了中国科学家郑兰荪院士首次成功合成新型稳定小富勒烯C50Cl10,外侧有10个氯原子,其形状酷似太空船(如图),有关C50Cl10的说法正确的是( )


| A、C50Cl10摩尔质量为955g |
| B、C50Cl10晶体是原子晶体 |
| C、C50Cl10分子中含有25个碳碳双键 |
| D、C50Cl10分子共用电子对数目为105对 |
在解释下列物质的性质变化规律与物质结构间的因果关系时,与键能无关的变化规律是( )
| A、与硅相比,金刚石的硬度大,熔点高 |
| B、HF、HCl、HBr、HI热稳定性依次减弱 |
| C、F2、Cl2、Br2、I2的沸点逐渐升高 |
| D、F2比O2更容易与H2反应 |





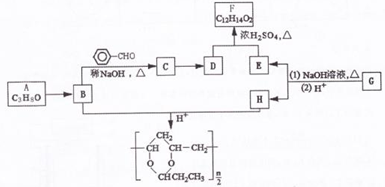
 +H2O(R、R′表示烃基或氢)
+H2O(R、R′表示烃基或氢)