题目内容
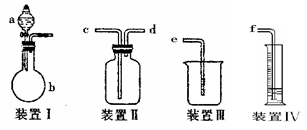
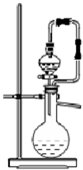 用如图装置不能完成气体制取任务的是
用如图装置不能完成气体制取任务的是
- A.过氧化钠和水反应制取氧气
- B.生石灰和浓氨水反应制取氨气
- C.二氧化锰和浓盐酸反应制取氯气
- D.碳化钙和饱和食盐水反应制取乙炔
分析:该装置适合固体和液体反应且不需加热制取气体,据此分析,并结合各选项进行解答.
解答:A.用过氧化钠(Na2O2)和水反应2Na2O2+2H2O═4NaOH+O2↑,该反应制取氧气属于固液常温型的反应,不需加热,可用此装置制取,故A正确;
B.浓氨水易挥发,CaO固体与水反应放出大量的热,导致温度升高,使得氨气在水中的溶解度进一步减少,以气体的形式逸出,制得氨气,所以能用图中的装置制备,故B正确;
C.实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O,反应需要加热不符合图中装置的要求,故C错误;
MnCl2+Cl2↑+2H2O,反应需要加热不符合图中装置的要求,故C错误;D.实验室常用碳化钙固体(俗称电石,化学式为CaC2)与水反应制备乙炔,同时生成氢氧化钙,该反应的化学方程式为CaC2+2H2O═Ca(OH)2+C2H2↑;属于固体和液体混合反应不需要加热的反应,所以能用图中的装置制备,故D正确;
故选C.
点评:本题主要考查了化学实验装置的选择,认真分析实验装置图的特点,准确读出图示信息是解题的关键,题目难度不大.

 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案药品:①2% NaOH溶液②稀HCl③稀H![]() SO
SO![]() ④饱和KHCO
④饱和KHCO![]() 溶液⑤浓H
溶液⑤浓H![]() SO
SO![]() ⑥CaCO
⑥CaCO![]() 固体⑦K
固体⑦K![]() CO
CO![]() 粉末
粉末
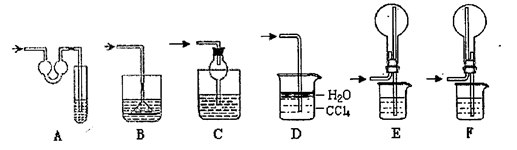
仪器装置(如图所示):
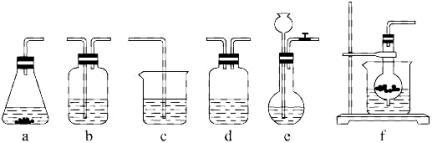
请根据题目要求完成下列问题:
请按下表要求,填写选择的装置和药品。
分项内容 | CO | 除杂洗气装置(Y) | 制备产品装置(Z) |
选择的装置 (填序号) |
|
| C |
选择的药品 (填序号) |
|
| ① |
(2)如何检验所选择的CO![]() 发生装置(X)的气密性,请写出主要操作过程:__________。
发生装置(X)的气密性,请写出主要操作过程:__________。
(3)将装置按X、Y、Z顺序连接并检查气密性后,当加入药品实验时,X装置中发生化学反应的离子方程式为_____________,Y装置中除去的杂质为_________________。
(4)常温下,向Z装置的NaOH溶液中通入过量CO2气体,其目的是______________。
(5)若要保证Z装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过________________%(质量分数)。
附:有关物质在常温(25 ℃)时的溶解度
化学式 | Na | NaHCO | NaOH | NaCl | Na |
溶解度 (g/100 g H | 21.3 | 9.60 | 107 | 35.8 | 19.4
|
某校化学研究性学习小组利用下面所提供的仪器装置和药品制取NaHCO3溶液,设计如下实验。实验室提供的药品、仪器装置如下:
药品:①2% NaOH溶液 ②稀HCl ③稀H2SO4 ④饱和KHCO3溶液 ⑤浓H2SO4 ⑥CaCO3固体 ⑦K2CO3粉末
仪器装置(如图所示):
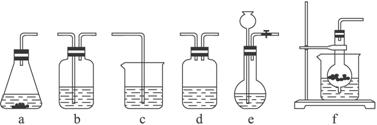
请根据题目要求完成下列问题:
(1)请按下表要求,填写选择的装置和药品。
| 分项 内容 | CO2发生装置(随开随用,随关随停)(X) | 除杂洗气装置(Y) | 制备产品装置(Z) |
| 选择的装置(填序号) | c | ||
| 选择的药品(填序号) | ① |
(2)如何检验所选择的CO2发生装置(X)的气密性,请写出主要操作过程:_________________。
(3)将装置按X、Y、Z顺序连接并检查气密性后,当加入药品实验时,X装置中发生化学反应的离子方程式为________________________,Y装置中除去的杂质为_____________。
(4)常温下,向Z装置的NaOH溶液中通入过量CO2气体,其目的是____________________。
(5)若要保证Z装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过_______________%(质量分数)。
附:有关物质在常温(25 ℃)时的溶解度
| 化学式 | Na2CO3 | NaHCO3 | NaOH | NaCl | Na2SO4 |
| 溶解度(g/100 g H2O) | 21.3 | 9.60 | 107 | 35.8 | 19.4 |
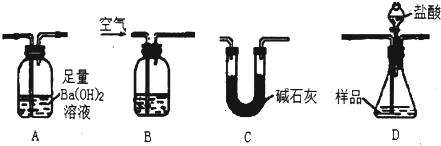

 置序号
置序号