题目内容
(2012?醴陵市模拟)实验室有一包暗红色粉末样品可能是CaCO3、Fe2O3或FeO的混合物.后经测定已确定不存在FeO.
I.某学生想自己设计实验方案,以证明样品中确实没有FeO.除样品外,实验室只提供以下试剂:KMnO4溶液、稀盐酸、稀硫酸、KSCN溶液、NaOH溶液和双氧水.你认为要完成该实验所选择的试剂是
Ⅱ.测定混合物中Fe2O3的含量
实验室可用多种方法测出上述样品中Fe2O3的质量分数.现有学生准备用如图各装置按一定顺序连接成一套完整的组合装置来进行实验以测定Fe2O3的质量分数.
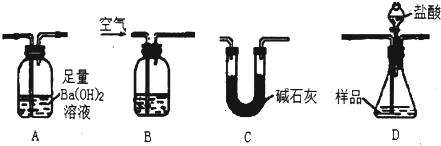
请根据题意回答下列问题:
(1)装置的连接顺序是
(2)实验过程中需要持续通入空气,其作用除可以起到“搅拌”A、D中反应物达到充分反应外,还有一个重要作用是
(3)下列各项措施中,能提高测定准确度的是
a.在加入盐酸之前,应该排尽装置内的CO2气体
b.快速加入盐酸
c.在B中装入浓硫酸
d.在B中装入NaOH溶液
e.D之后增添盛有饱和碳酸氢钠溶液的洗气装置
(4)实验室准确称取26.0g固体样品装入D中,充分反应后,测得A中沉淀质量为19.7g,则样品中Fe2O3的质量分数为
(5)在进行实验方案评价时,有学生认为不必测定A中的沉淀质量,而只要测出装置A在吸收反应产生的气体前后的质量差,就能完成实验要求.实验证明,若用此法测得Fe2O3的质量分数将
I.某学生想自己设计实验方案,以证明样品中确实没有FeO.除样品外,实验室只提供以下试剂:KMnO4溶液、稀盐酸、稀硫酸、KSCN溶液、NaOH溶液和双氧水.你认为要完成该实验所选择的试剂是
KMnO4溶液、稀硫酸
KMnO4溶液、稀硫酸
,请你描述实验操作时的步骤、实验现象和结论:取少量样品溶于试管中,配成溶液后,再滴入几滴稀硫酸和几滴KMnO4溶液,只要溶液不褪色或不变浅,即说明样品中无FeO
取少量样品溶于试管中,配成溶液后,再滴入几滴稀硫酸和几滴KMnO4溶液,只要溶液不褪色或不变浅,即说明样品中无FeO
.Ⅱ.测定混合物中Fe2O3的含量
实验室可用多种方法测出上述样品中Fe2O3的质量分数.现有学生准备用如图各装置按一定顺序连接成一套完整的组合装置来进行实验以测定Fe2O3的质量分数.

请根据题意回答下列问题:
(1)装置的连接顺序是
BDAC
BDAC
(填字母,每个装置只能用一次)(2)实验过程中需要持续通入空气,其作用除可以起到“搅拌”A、D中反应物达到充分反应外,还有一个重要作用是
将反应产生的CO2气体尽可能彻底的赶入装置A中,使之完全被Ba(OH)2溶液吸收
将反应产生的CO2气体尽可能彻底的赶入装置A中,使之完全被Ba(OH)2溶液吸收
(3)下列各项措施中,能提高测定准确度的是
ad
ad
(填标号)a.在加入盐酸之前,应该排尽装置内的CO2气体
b.快速加入盐酸
c.在B中装入浓硫酸
d.在B中装入NaOH溶液
e.D之后增添盛有饱和碳酸氢钠溶液的洗气装置
(4)实验室准确称取26.0g固体样品装入D中,充分反应后,测得A中沉淀质量为19.7g,则样品中Fe2O3的质量分数为
61.5%
61.5%
.(5)在进行实验方案评价时,有学生认为不必测定A中的沉淀质量,而只要测出装置A在吸收反应产生的气体前后的质量差,就能完成实验要求.实验证明,若用此法测得Fe2O3的质量分数将
偏低
偏低
(填“偏高”、“偏低”、“不变”)分析:Ⅰ.若Fe2O3中含有FeO,利用稀酸(非氧化性)溶解后生成的亚铁离子,则具有还原性,而给出的试剂中KMnO4溶液具有强氧化性,可利用KMnO4溶液褪色来证明;根据检验方法写出实验操作时的步骤、实验现象和结论;
Ⅱ.(1)先分析实验方案,利用装置B除去空气中的二氧化碳,然后用空气将装置D产生的二氧化碳完全赶到装置A中,为了避免空气中水和二氧化碳干扰,装置A需要连接吸收二氧化碳和水的装置,据此对装置进行排序;
(2)根据通入空气还可以将碳酸钙与盐酸反应生成的二氧化碳驱赶到装置B中分析;
(3)a、根据该实验是通过测定二氧化碳的质量进行计算样品中氧化铁的质量分数的分析;
b、加入的盐酸速度过快,会导致二氧化碳与氢氧化钡溶液反应不完全;
c、装置B中装入浓硫酸,浓硫酸不能够吸收空气中的二氧化碳,导致测定的二氧化碳质量偏大;
d、B中使用氢氧化钠溶液,目的是吸收空气中的二氧化碳;
e、由于是通过测定碳酸钡质量来计算生成二氧化碳的质量的,二氧化碳中的氯化氢不影响测定结果;
(4)装置A中的沉淀为碳酸钡,根据关系式和碳酸钡的质量计算出碳酸钙的质量,再计算出样品中氧化铁的质量分数;
(5)由于反应生成的二氧化碳中含有杂质氯化氢和水,导致测定的装置A的质量差增大,测定碳酸钙质量偏大,氧化铁的质量分数偏低.
Ⅱ.(1)先分析实验方案,利用装置B除去空气中的二氧化碳,然后用空气将装置D产生的二氧化碳完全赶到装置A中,为了避免空气中水和二氧化碳干扰,装置A需要连接吸收二氧化碳和水的装置,据此对装置进行排序;
(2)根据通入空气还可以将碳酸钙与盐酸反应生成的二氧化碳驱赶到装置B中分析;
(3)a、根据该实验是通过测定二氧化碳的质量进行计算样品中氧化铁的质量分数的分析;
b、加入的盐酸速度过快,会导致二氧化碳与氢氧化钡溶液反应不完全;
c、装置B中装入浓硫酸,浓硫酸不能够吸收空气中的二氧化碳,导致测定的二氧化碳质量偏大;
d、B中使用氢氧化钠溶液,目的是吸收空气中的二氧化碳;
e、由于是通过测定碳酸钡质量来计算生成二氧化碳的质量的,二氧化碳中的氯化氢不影响测定结果;
(4)装置A中的沉淀为碳酸钡,根据关系式和碳酸钡的质量计算出碳酸钙的质量,再计算出样品中氧化铁的质量分数;
(5)由于反应生成的二氧化碳中含有杂质氯化氢和水,导致测定的装置A的质量差增大,测定碳酸钙质量偏大,氧化铁的质量分数偏低.
解答:解:Ⅰ.若Fe2O3中含有FeO,利用稀酸(非氧化性)溶解后生成的亚铁离子,则具有还原性,而给出的试剂中KMnO4溶液具有强氧化性,可使KMnO4溶液褪色,
则选择试剂为稀硫酸、KMnO4溶液;实验操作时的步骤、实验现象和结论为:取少量样品溶于试管中,配成溶液后,再滴入几滴稀硫酸和几滴KMnO4溶液,只要溶液不褪色或不变浅,即说明样品中无FeO,
故答案为:KMnO4溶液、稀硫酸;取少量样品溶于试管中,配成溶液后,再滴入几滴稀硫酸和几滴KMnO4溶液,只要溶液不褪色或不变浅,即说明样品中无FeO;
Ⅱ.(1)测定样品中Fe2O3的质量分数,先根据碳酸钙产生的二氧化碳的质量计算出碳酸钙的质量,再根据样品质量计算出氧化铁的质量分数,仪器连接顺序为:先将空气通入盛有氢氧化钠溶液的装置B,以便除去空气中的二氧化碳,然后利用空气将装置D中产生的二氧化碳驱赶到装置A,利用二氧化碳与氢氧化钡生成的碳酸钡沉淀的质量计算出碳酸钙的质量,由于空气中的二氧化碳、水蒸气影响测定结果,需要在装置A后连接一个吸收二氧化碳、水蒸气的装置C,所以装置连接顺序为:BDAC,
故答案为:BDAC;
(2)实验过程中需要持续通入空气,其作用除可以起到“搅拌”A、D中反应物达到充分反应外,还可以使反应生成的二氧化碳尽可能彻底的赶入装置A中,使反应生成的二氧化碳能够被氢氧化钡溶液完全吸收,
故答案为:将反应产生的CO2气体尽可能彻底的赶入装置A中,使之完全被Ba(OH)2溶液吸收;
(3)a、该实验是通过测定二氧化碳的质量来计算样品中氧化铁的质量分数的,在加入盐酸之前,应该排尽装置内的CO2气体,避免装置中的二氧化碳影响测定结果,故a正确;
b、若加入的盐酸速度过快,二氧化碳与氢氧化钡溶液反应不完全,导致测定的二氧化碳的质量偏低,样品中碳酸钙的质量偏小,影响了测定结果,故b错误;
c、若装置B中装入浓硫酸,由于浓硫酸不能够吸收二氧化碳,导致空气中的二氧化碳被氢氧化钡溶液吸收,导致测定的二氧化碳质量偏大,应该使用氢氧化钠溶液,故c错误;
d、装置B中盛有氢氧化钠溶液,目的是为了吸收空气中的二氧化碳,避免空气中的二氧化碳影响测定结果,故d正确;
e、由于该实验是通过测定碳酸钡质量来计算生成二氧化碳的质量,二氧化碳中的氯化氢不影响测定结果,没有必要在D之后增添盛有饱和碳酸氢钠溶液的洗气装置,故e错误;
故选ad;
(4)由CaCO3+2HCl═CaCl2+H2O+CO2↑、CO2+Ba(OH)2=BaCO3↓+H2O可知,CaCO3~BaCO3,
设碳酸钙的质量为x,
CaCO3→BaCO3,
100 197
x 19.7g
解得:x=10g,样品中氧化铁的质量为:26g-10g=16g,
样品中Fe2O3的质量分数为:
×100%=61.5%,
故答案为:61.5%;
(5)由于装置D生成的二氧化碳中混有氯化氢和水,导致装置A在吸收反应产生的气体前后的质量差偏大,测定的二氧化碳的质量偏大,碳酸钙的质量会偏大,样品中氧化铁的质量偏小,氧化铁的质量分数会偏低,
故答案为:偏低.
则选择试剂为稀硫酸、KMnO4溶液;实验操作时的步骤、实验现象和结论为:取少量样品溶于试管中,配成溶液后,再滴入几滴稀硫酸和几滴KMnO4溶液,只要溶液不褪色或不变浅,即说明样品中无FeO,
故答案为:KMnO4溶液、稀硫酸;取少量样品溶于试管中,配成溶液后,再滴入几滴稀硫酸和几滴KMnO4溶液,只要溶液不褪色或不变浅,即说明样品中无FeO;
Ⅱ.(1)测定样品中Fe2O3的质量分数,先根据碳酸钙产生的二氧化碳的质量计算出碳酸钙的质量,再根据样品质量计算出氧化铁的质量分数,仪器连接顺序为:先将空气通入盛有氢氧化钠溶液的装置B,以便除去空气中的二氧化碳,然后利用空气将装置D中产生的二氧化碳驱赶到装置A,利用二氧化碳与氢氧化钡生成的碳酸钡沉淀的质量计算出碳酸钙的质量,由于空气中的二氧化碳、水蒸气影响测定结果,需要在装置A后连接一个吸收二氧化碳、水蒸气的装置C,所以装置连接顺序为:BDAC,
故答案为:BDAC;
(2)实验过程中需要持续通入空气,其作用除可以起到“搅拌”A、D中反应物达到充分反应外,还可以使反应生成的二氧化碳尽可能彻底的赶入装置A中,使反应生成的二氧化碳能够被氢氧化钡溶液完全吸收,
故答案为:将反应产生的CO2气体尽可能彻底的赶入装置A中,使之完全被Ba(OH)2溶液吸收;
(3)a、该实验是通过测定二氧化碳的质量来计算样品中氧化铁的质量分数的,在加入盐酸之前,应该排尽装置内的CO2气体,避免装置中的二氧化碳影响测定结果,故a正确;
b、若加入的盐酸速度过快,二氧化碳与氢氧化钡溶液反应不完全,导致测定的二氧化碳的质量偏低,样品中碳酸钙的质量偏小,影响了测定结果,故b错误;
c、若装置B中装入浓硫酸,由于浓硫酸不能够吸收二氧化碳,导致空气中的二氧化碳被氢氧化钡溶液吸收,导致测定的二氧化碳质量偏大,应该使用氢氧化钠溶液,故c错误;
d、装置B中盛有氢氧化钠溶液,目的是为了吸收空气中的二氧化碳,避免空气中的二氧化碳影响测定结果,故d正确;
e、由于该实验是通过测定碳酸钡质量来计算生成二氧化碳的质量,二氧化碳中的氯化氢不影响测定结果,没有必要在D之后增添盛有饱和碳酸氢钠溶液的洗气装置,故e错误;
故选ad;
(4)由CaCO3+2HCl═CaCl2+H2O+CO2↑、CO2+Ba(OH)2=BaCO3↓+H2O可知,CaCO3~BaCO3,
设碳酸钙的质量为x,
CaCO3→BaCO3,
100 197
x 19.7g
解得:x=10g,样品中氧化铁的质量为:26g-10g=16g,
样品中Fe2O3的质量分数为:
| 16g |
| 26g |
故答案为:61.5%;
(5)由于装置D生成的二氧化碳中混有氯化氢和水,导致装置A在吸收反应产生的气体前后的质量差偏大,测定的二氧化碳的质量偏大,碳酸钙的质量会偏大,样品中氧化铁的质量偏小,氧化铁的质量分数会偏低,
故答案为:偏低.
点评:本题考查了测定物质的组成,题目难度较大,涉及的内容较多,注意明确亚铁离子具有还原性是检验氧化亚铁存在的关键,注意根据实验现象和结论的关系来解答,本题在注重对学生基础知识训练和检验的同时,侧重对学生实验答题能力的培养和方法与技巧的指导和训练,有利于提高学生的实验设计能力和应试能力,提升学生的学科素养.

练习册系列答案
相关题目
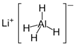 )、LiH是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al.下列说法不正确的是( )
)、LiH是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al.下列说法不正确的是( )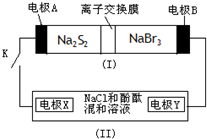 (2012?醴陵市模拟)如图所示,装置(Ⅰ)是一种可充电电池,装置(Ⅱ)为电解池,装置(Ⅰ)的离子交换膜只允许Na+通过.电池充、放电的化学方程式为:
(2012?醴陵市模拟)如图所示,装置(Ⅰ)是一种可充电电池,装置(Ⅱ)为电解池,装置(Ⅰ)的离子交换膜只允许Na+通过.电池充、放电的化学方程式为: