题目内容
【题目】高铁酸盐具有极强的氧化性,可作水处理剂。低温下,在Na2FeO4溶液中加入KOH浓溶液可析出K2FeO4。完成下列填空:
(1)写出上述得到K2FeO4的化学方程式_____。
(2)Na2FeO4和稀H2SO4发生如下反应:Na2FeO4+H2SO4→Fe2(SO4)3+O2↑+Na2SO4+H2O。配平上述化学方程式_____。若反应中产生3.36L(标准状况)的氧气,则转移电子数为_____。
(3)实验室配制Fe2(SO4)3溶液时,需加入少量稀硫酸,结合离子方程式用化学平衡移动原理解释其原因______。
(4)在Fe2(SO4)3溶液中滴加NaHSO3溶液,n(SO42-)增大,则还原产物是____。写出检验上述反应中Fe2(SO4)3是否消耗完全的方法______。
(5)已知HSO3-在水中既能水解也能电离。NaHSO3溶液呈酸性,溶液中c(H2SO3)_____c(SO32-)(选填“>”、“<”或“=”)。
【答案】Na2FeO4+2KOH=K2FeO4+2NaOH 4Na2FeO4+10H2SO4=2Fe2(SO4)3+3O2↑+4Na2SO4+10H2O 0.6NA Fe3+易水解:Fe3++3H2O![]() Fe(OH)3+3H+,加入少量稀硫酸可使水解平衡逆向移动,抑制其水解,减少损耗 FeSO4 取少量溶液于试管中,向试管中加入KSCN溶液,若溶液不变红,则证明Fe2(SO4)3消耗完全,若溶液变成红色,Fe2(SO4)3未消耗完全 <
Fe(OH)3+3H+,加入少量稀硫酸可使水解平衡逆向移动,抑制其水解,减少损耗 FeSO4 取少量溶液于试管中,向试管中加入KSCN溶液,若溶液不变红,则证明Fe2(SO4)3消耗完全,若溶液变成红色,Fe2(SO4)3未消耗完全 <
【解析】
(1)根据题干信息写出化学反应方程式;
(2)根据氧化还原反应规律,得失电子守恒进行方程式的配平和相关计算;
(3)Fe3+易水解,加入少量稀硫酸可抑制其水解,从此角度进行分析解答;
(4)结合氧化还原反应分析问题,检验Fe3+用KSCN溶液;
(5)根据溶液的酸碱性判断HSO3-的电离程度和水解程度相对大小,从而判断粒子浓度大小关系。
(1)由题干信息可知,低温下,在Na2FeO4溶液中加入KOH浓溶液可析出K2FeO4,化学反应方程式为Na2FeO4+2KOH=K2FeO4+2NaOH,故答案为:Na2FeO4+2KOH=K2FeO4+2NaOH;
(2)Na2FeO4和稀H2SO4发生如下反应:Na2FeO4+H2SO4→Fe2(SO4)3+O2↑+Na2SO4+H2O,反应中Na2FeO4的Fe元素的化合价由+6价降低至+3价,反应中O元素的化合价由-2价升高至0价,根据氧化还原反应得失电子守恒配平可得反应方程式为4Na2FeO4+10H2SO4=2Fe2(SO4)3+3O2↑+4Na2SO4+10H2O,反应中每生成1molO2转移4mol电子,标况下3.36LO2的物质的量为0.15mol,则转移的电子为0.15mol×4=0.6mol,数目为0.6NA,故答案为:4Na2FeO4+10H2SO4=2Fe2(SO4)3+3O2↑+4Na2SO4+10H2O;0.6NA;
(3)Fe2(SO4)3溶液中Fe3+易水解:Fe3++3H2O![]() Fe(OH)3+3H+,加入少量稀硫酸可使水解平衡逆向移动,抑制其水解,减少损耗,故答案为:Fe3+易水解:Fe3++3H2O
Fe(OH)3+3H+,加入少量稀硫酸可使水解平衡逆向移动,抑制其水解,减少损耗,故答案为:Fe3+易水解:Fe3++3H2O![]() Fe(OH)3+3H+,加入少量稀硫酸可使水解平衡逆向移动,抑制其水解,减少损耗;
Fe(OH)3+3H+,加入少量稀硫酸可使水解平衡逆向移动,抑制其水解,减少损耗;
(4)在Fe2(SO4)3溶液中滴加NaHSO3溶液,n(SO42-)增大,发生反应:2Fe3++HSO3-+H2O=SO42-+2Fe2++3H+,Fe3+被还原成Fe2+,故还原产物为FeSO4,检验上述反应中Fe2(SO4)3是否消耗完全即检验溶液中是否还存在着Fe3+,可用KSCN溶液进行检验,具体方法为:取少量溶液于试管中,向试管中加入KSCN溶液,若溶液不变红,则证明Fe2(SO4)3消耗完全,若溶液变成红色,Fe2(SO4)3未消耗完全,故答案为:FeSO4;取少量溶液于试管中,向试管中加入KSCN溶液,若溶液不变红,则证明Fe2(SO4)3消耗完全,若溶液变成红色,Fe2(SO4)3未消耗完全;
(5)NaHSO3溶液呈酸性,则HSO3-的电离程度大于水解程度,则水解产生的H2SO3的浓度小于电离生成的SO32-的浓度,故答案为:<。

【题目】某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、乙酸。

已知:①无水氯化钙可与乙醇形成微溶于水的CaCl2·6C2H5OH;
②有关有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
请回答:
(1)圆底烧瓶中发生的化学反应方程式:________,浓硫酸的作用为________。
(2)球形干燥管C的作用是_________,D中放________溶液,其作用是________。
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出____________;再加入(此空从下列选项中选择)__________;然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯。
A.生石灰B.碱石灰C.无水硫酸钠
【题目】某化学小组探究酸性条件下NO3-、SO42-、Fe3+三种微粒的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
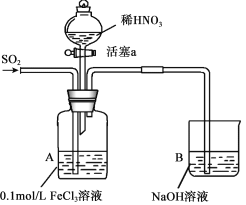
实验记录如下:
实验序号 | 实验操作 | 实验现象 |
I | 向A装置中通入一段时间的SO2气体。 | A中黄色溶液迅速变成深红棕色,最终变为浅绿色。 |
II | 取出少量A装置中的溶液,先加入KSCN溶液,再加入BaCl2溶液。 | 加入KSCN溶液后溶液不变色,再加入BaCl2溶液产生白色沉淀。 |
III | 打开活塞a,将过量稀HNO3加入装置A中,关闭活塞a。 | A中浅绿色溶液最终变为黄色。 |
IV | 取出少量A装置中的溶液,加入KSCN溶液;向A装置中注入空气。 | 溶液变为红色;液面上方有少量红棕色气体生成。 |
请回答下列问题:
(1)配制FeCl3溶液时,常常加入盐酸,目的是(用化学用语和简单文字叙述):________。
(2)资料表明,Fe3+能与SO2结合形成深红棕色物质Fe(SO2)63+,反应方程式为: Fe3+ + 6SO2 ![]() Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因________。
Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因________。
(3)实验II中发生反应的离子方程式是__________________。
(4)实验III中,浅绿色溶液变为黄色的原因是__________________(用离子方程式表示)。
(5)实验IV中液面上方有少量红棕色气体生成,发生反应的化学方程式是______________。
(6)综合上述实验得出的结论是:在酸性条件下,氧化性强弱是:NO3->Fe3+>SO42-。请从微粒变化的角度解释________。







