题目内容
某液态化合物X2Y4,常用作火箭燃料。32g X2Y4在一定量的O2中恰好完全燃烧,反应方程式为X2Y4(l)+O2(g) X2(g)+2Y2O(l)。冷却后在标准状况下测得生成物的体积为22.4 L,其密度为1.25 g·L-1,则:
X2(g)+2Y2O(l)。冷却后在标准状况下测得生成物的体积为22.4 L,其密度为1.25 g·L-1,则:
(1)反应前O2在标准状况的体积 V(O2)约为________L;
V(O2)约为________L;
(2)X2的摩尔质量为________________,Y元素的名称是______________;
(3)若反应生成0.1 mol X2,则生成Y2O的质量为________g。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某硝酸钠固体中混有少量硫酸铵和硫酸镁杂质,现设计一实验方案,既除去杂质,又配成硝酸钠溶液。实验方案:先将固体溶于蒸馏水配成溶液,选择合适的试剂和操作完成表格中各步实验。(已知NH4++OH- 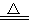 NH3↑+H2O)
NH3↑+H2O)
选择试剂 | ① | Na2CO3溶液 | ② |
实验操作 | ③ | ④ | 调节pH |
下列试剂或操作不合理的是
A.试剂①为Ba(OH)2溶液 B.试剂②为稀HNO3
C.操作③为结晶 D.操作为④过滤


 2CO3——HCl
2CO3——HCl
 O2(g)= H2O(g) ΔH=-10a kJ·mol-1
O2(g)= H2O(g) ΔH=-10a kJ·mol-1 2NH3(g) ΔH=-38.6kJ·mol-1。将分子数为1.5NA的H2和过量N2在此条件下充分反应,放出热量19.3 kJ
2NH3(g) ΔH=-38.6kJ·mol-1。将分子数为1.5NA的H2和过量N2在此条件下充分反应,放出热量19.3 kJ