题目内容
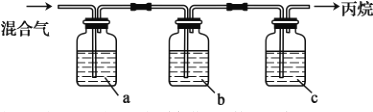
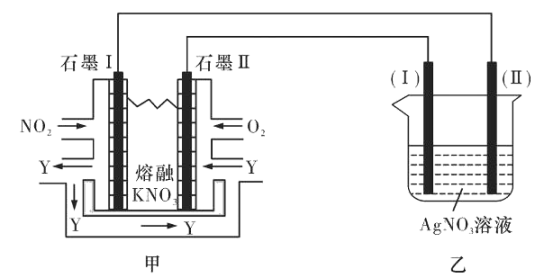
【题目】下图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色色斑向d端扩散。下列判断正确的是( )

A.滤纸上c点附近会变红色
B.Cu电极质量减小,Pt电极质量增大
C.烧杯中溶液的pH先减小,后增大
D.Z溶液中SO42-向Cu电极定向移动
【答案】A
【解析】
由图可知,为电解装置,由通电后Y中央的紫红色色斑向d端扩散,则d为阳极极,b为电源的正极,a为负极,则Cu电极上铜离子得到电子,Pt电极上氢氧根离子失去电子,以此来解答。
A.Y为浸透饱和食盐水和酚酞试液的滤纸,c点氢离子放电,则氢氧根离子浓度增大,所以滤纸上c点附近会变红色,A正确;
B.Cu电极上铜离子得到电子,Pt电极上氢氧根离子失去电子,则Cu电极质量增大,Pt电极不变,B错误;
C.Pt电极上氢氧根离子失去电子,则烧杯中溶液的pH减小,C错误;
D.Cu电极为阴极,则烧杯中溶液中SO42-向Pt电极定向移动,D错误;
答案选A。

【题目】炼锌厂的铜镉废渣中含有铜、锌、镉、铁、砷等元素,其含量依次减少。对这些元素进行提取分离会减小环境污染,同时制得ZnSO4·7H2O实现资源的再利用,其流程图如下。已知FeAsO4难溶于水和酸;ZnSO4·7H2O易溶于水,难溶于酒精。
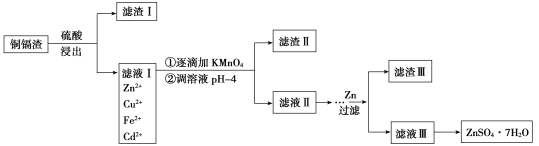
常温下金属离子沉淀的pH
金属离子 | Fe3+ | Zn2+ | Mn2+ | Cu2+ | Cd2+ |
开始沉淀pH | 2.7 | 6.5 | 7.7 | 5.2 | 6.9 |
沉淀完全pH | 3.2 | 8.0 | 9.8 | 6.4 | 9.4 |
请回答下列问题:
(1)提高浸出速率可以采用的方法是(写出其中一点即可)________。
(2)滤液Ⅰ中有少量AsO33—,若不除去,则AsO33—与Cd反应会产生一种有毒氢化物气体,其分子式为____,向滤液Ⅰ中逐滴滴入酸性KMnO4溶液可与AsO33—反应生成FeAsO4,完成并配平下列反应的离子方程式___:Fe2++AsO33—+MnO4—+___=FeAsO4↓+Mn2++__,判断该滴定终点的现象是__________。
(3)流程中②调节pH时可以选用的试剂为________,滤渣Ⅱ的成分为________。
(4)常温下Zn(OH)2的溶度积Ksp=________。
(5)制得的ZnSO4·7H2O需洗涤,洗涤晶体时可选用试剂为________。