题目内容
【题目】H、C、N、O、Na、S是常见的六种元素。请回答下列问题。
(1)S在元素周期表中的位置为______________。
(2)上述元素中非金属性最强的是______________(填元素符号)。
(3)下列事实能说明O的非金属性比S的非金属性强的是________(填字母代号)。
a.O2与H2S溶液反应,溶液变浑浊
b.加热条件下H2S比H2O更容易分解
c.在氧化还原反应中,1 mol O2比1 mol S得电子多
d.H2O的沸点比H2S高
(4)一定条件下,Na还原CCl4可得到金刚石与一种可溶性盐,该反应的化学方程式为_________________。
(5)肼(N2H4)是一种无色易溶于水的油状液体。其具有碱性和极强的还原性,在工业生产中应用非常广泛。
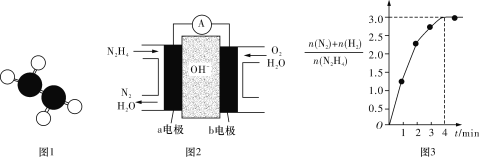
①已知肼的球棍模型如图1所示,试写出肼的电子式:______________。
②目前正在研发的一种肼燃料电池的结构如图2所示,________(填“a”或“b”)电极为电池的负极。
③在1 L固定体积的密闭容器中加入0.1 mol N2H4,在303 K、Pt催化下发生反应N2H4(l) ![]() N2(g)+2H2(g),测得容器中的与时间的关系如图3所示,则 0~4 min内氮气的平均反应速率v(N2)=____________。
N2(g)+2H2(g),测得容器中的与时间的关系如图3所示,则 0~4 min内氮气的平均反应速率v(N2)=____________。
【答案】 第三周期第ⅥA族 O ab CCl4+4Na![]() 4NaCl+C(金刚石)
4NaCl+C(金刚石) ![]() a 0.012 5 mol·L-1·min-1
a 0.012 5 mol·L-1·min-1
【解析】(1)根据S的原子序数为16分析解答;
(2)在周期表中,元素金属性最强的元素位于周期表左下角,非金属性最强的元素位于周期表右上角。据此分析判断;
(3)根据元素非金属性强弱的比较方法分析判断;
(4)一定条件下,Na还原CCl4可得到金刚石与一种可溶性盐,根据元素守恒,该盐为氯化钠,据此书写;
(5)①氨分子中氢原子被氨基(-NH2)取代后的生成物叫肼,据此书写;②根据正极是氧气得电子发生还原反应,负极肼失电子发生氧化反应判断;③在303K,Pt催化下,则发生N2H4(l)N2(g)+2H2(g),设生成氮气的量为xmol,则氢气的量为:2xmol,此时N2H4(l)的物质的量为(1-x)mol,根据4min时比值为3,求出x的值,然后根v=![]() 计算。
计算。
(1)S的原子序数为16,核外含有3个电子层,最外层含有6个电子,位于周期表中第三周期ⅥA族;故答案为:第三周期ⅥA族;
(2)在周期表中,元素金属性最强的元素位于周期表左下角,非金属性最强的元素位于周期表右上角,所以非金属性最强的元素是O,故答案为:O;
(3)a.O2与H2S溶液反应,溶液变浑浊,氧气与硫化氢反应生成硫沉淀,说明O元素的非金属性比S强,故a正确;b.O和S两元素的简单氢化物受热分解,前者的分解温度高,说明水比硫化氢稳定,即O元素的非金属性比S强,故b正确;c.在氧化还原反应中,得电子能力越强,元素的非金属性越强,与得电子多少无关,故c错误;d.沸点是物理性质,与非金属性强弱无关,故d错误;故答案为:ab;
(4)一定条件下,Na还原CCl4可得到金刚石与一种可溶性盐,为氯化钠,反应的化学方程式为CCl4+4Na![]() 4NaCl+C(金刚石),故答案为:CCl4+4Na
4NaCl+C(金刚石),故答案为:CCl4+4Na![]() 4NaCl+C(金刚石);
4NaCl+C(金刚石);
(5)①氨分子中氢原子被氨基(-NH2)取代后的生成物叫肼,分子中全部为单键,电子式为:![]() ,故答案为:
,故答案为:![]() ;
;
②正极是氧气得电子发生还原反应,负极肼失电子发生氧化反应,所以a电极为电池的负极,故答案为:a;
③在303K,Pt催化下,则发生N2H4(l)N2(g)+2H2(g),设生成氮气的量为xmol,则氢气的量为:2xmol,此时N2H4(l)的物质的量为(0.1-x)mol,根据4min时比值为3,所以![]() =3,则x=0.05mol,v=
=3,则x=0.05mol,v=![]() =
=![]() =0.0125molL-1min-1,故答案为:0.0125molL-1min-1。
=0.0125molL-1min-1,故答案为:0.0125molL-1min-1。

【题目】下列六个说法中,正确的有
①已知2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1,则氢气的燃烧热为ΔH=-241.8 kJ·mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g) ![]() Z(g)+W(g) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
Z(g)+W(g) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
④已知:
共价键 | C—C | C=C | C—H | H—H |
键能/(kJ·mol-1) | 348 | 610 | 413 | 436 |
根据上表数据可以计算出C6H6(g)+3H2(g)→C6H12(g)的焓变
⑤根据盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1 mol CO2固体时,放出的热量相等
⑥25 ℃、101 kPa时,1 mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热
A. 1个 B. 2个 C. 3个 D. 4个
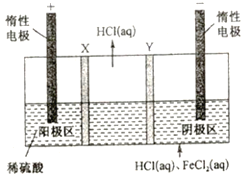
【题目】二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺. 
(1)①如图装置用石墨作电极,在一定条件下电解饱和食盐水制取ClO2 . 写出阳极产生ClO2的电极反应式: . ②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解.通过阳离子交换膜的阳离子的物质的量为mol.
(2)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2﹣离子.电池工作时正极反应为 .
(3)若以该电池为电源,用石墨做电极电解100mL含有如下离子的溶液.
离子 | Cu2+ | H+ | Cl﹣ | SO42﹣ |
c/molL﹣1 | 1 | 4 | 4 | 1 |
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的物质的量为mol.