题目内容
下列叙述与对应图式正确的是( )
 |
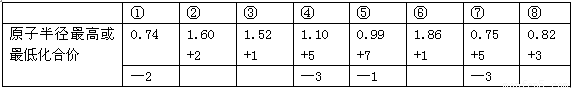
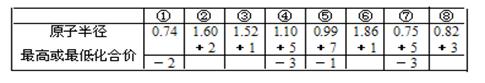
分析:A.由元素的原子半径和化合价可知③⑥为ⅠA族元素,③为Li,⑥为Na;
B.根据燃烧热的定义判断;
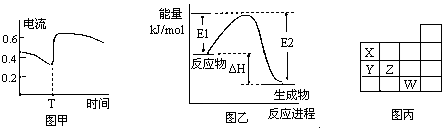
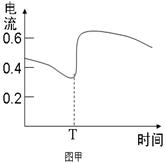
C.T时电流强度变大,说明单位时间内Zn被氧化的速率增大;
D.使用催化剂,反应热不变.
B.根据燃烧热的定义判断;
C.T时电流强度变大,说明单位时间内Zn被氧化的速率增大;
D.使用催化剂,反应热不变.
解答:解:A.由元素的原子半径和化合价可知③⑥为ⅠA族元素,③为Li,⑥为Na,则碱性较强的应为NaOH,故A错误;
B.燃烧热应是1mol纯净物完全燃烧生成稳定的氧化物放出的热量,应为1mol氢气,故B错误;
C.T时电流强度变大,说明单位时间内Zn被氧化的速率增大,加入H2O2,具有强氧化性,可加快锌的氧化,故C正确;
D.使用催化剂,降低反应的活化能,但反应热不变,故D错误.
故选C.
B.燃烧热应是1mol纯净物完全燃烧生成稳定的氧化物放出的热量,应为1mol氢气,故B错误;
C.T时电流强度变大,说明单位时间内Zn被氧化的速率增大,加入H2O2,具有强氧化性,可加快锌的氧化,故C正确;
D.使用催化剂,降低反应的活化能,但反应热不变,故D错误.
故选C.
点评:本题考查较为综合,涉及原子结构与元素周期律、燃烧热、原电池以及化学反应与能量变化,侧重于学生的分析能力的考查,为高考常见题型,注意原子结构与元素周期律的关系,把握燃烧热的定义,难度中等.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
下列叙述与对应图式正确的是( )

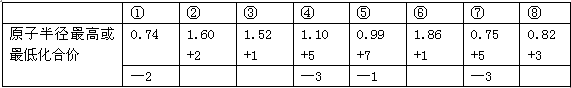
A、由下列短周期元素性质的数据推断元素③最高价氧化物对应的水化物碱性最强
| |||||||||||||||||||||||||||
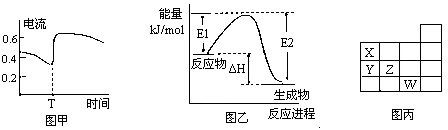
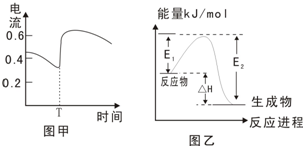
| B、图甲表示Zn-Cu原电池反应过程中的电流强度的变化.T时可能加入了H2O2 | |||||||||||||||||||||||||||
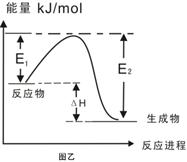
| C、图乙表示某一放热反应,若使用催化剂E1、E2、△H都会发生改变 | |||||||||||||||||||||||||||
| D、图丙表示元素周期表的一部分,元素X,Y,Z、W中X的氢化物酸性最强 |