题目内容
1.下列有关离子(或物质)的检验及结论正确的是( )| A. | 用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中含有K+ | |
| B. | 向无色溶液中加入BaCl2溶液有白色沉淀出现,则溶液中含有SO42ˉ | |
| C. | 用一束光照射氯化铁溶液和氢氧化铁胶体,都出现丁达尔现象 | |
| D. | 向某溶液中加入NaOH溶液后再加热,若产生的气体能使湿润红色石蕊试纸变蓝,则该溶液中肯定有NH4+ |
分析 A.应通过蓝色钴玻璃观察钾的焰色反应;
B.不能排除AgCl沉淀的干扰;
C.只有胶体具有丁达尔效应;
D.和氢氧化钠反应生成氨气的离子是铵根离子.
解答 解:A.钠的焰色为黄色,则用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中一定含Na+,还可能含有K+,故A错误;
B.溶液中加入氯化钡溶液有白色沉淀,再加入盐酸,沉淀不溶解,则溶液中含有SO42-离子或者是SO32-离子或Ag+离子,故B错误;
C.只有胶体具有丁达尔效应,故C错误;
D.溶液中加入氢氧化钠溶液,加热后能产生使湿润的红色石蕊试纸变蓝的气体即氨气,则溶液中含有NH4+,故D正确.
故选D.
点评 本题考查物质的鉴别,为高频考点,题目难度中等,涉及焰色反应、离子检验及碘的特性等知识,把握物质性质及实验原理为解答的关键,注意发生的化学反应及反应现象.

练习册系列答案
相关题目
11.已知糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质.请结合题意回答问题:
(1)燃料乙醇的生产过程可表示如下:玉米→粉碎→水解→发酵→过滤→a→乙醇
①粉碎玉米的目的是增大反应物的接触面积或加快反应速率或使反应充分进行.
②生产过程中若想证明淀粉部分水解的实验方法是取少许水解后的液体分别置于两试管中,一支加入氢氧化钠溶液使其pH大于7,再加入新制的氢氧化铜悬浊液,加热,产生砖红色沉淀,证明淀粉发生了水解,产生葡萄糖;另一支加入少量碘水,碘水变蓝,证明还有未水解的淀粉存在.
③步骤a的操作是C.
A.蒸发 B.萃取 C.蒸馏 D分液.
(2)除去下列物质中的少量杂质(括号内为杂质),试填下表
(3)根据三种营养物质的性质,判断下列说法正确的是B.
A.蔗糖和麦芽糖互为同分异构体,二者均能与银氨溶液反应,并且水解产物相同.
B.盐析可提纯蛋白质并保持其生理活性.
C.天然植物油常温下一般呈液态,难溶于水,有固定的熔点、沸点.
D.两分子半胱氨酸(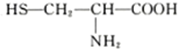 )脱水缩合形成二肽的结构简式为:
)脱水缩合形成二肽的结构简式为: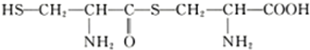 .
.
(4)写出工业上由硬脂酸甘油酯制肥皂的化学方程式: +3NaOH $\stackrel{加热}{→}$3C17H35COONa+
+3NaOH $\stackrel{加热}{→}$3C17H35COONa+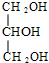 .
.
(1)燃料乙醇的生产过程可表示如下:玉米→粉碎→水解→发酵→过滤→a→乙醇
①粉碎玉米的目的是增大反应物的接触面积或加快反应速率或使反应充分进行.
②生产过程中若想证明淀粉部分水解的实验方法是取少许水解后的液体分别置于两试管中,一支加入氢氧化钠溶液使其pH大于7,再加入新制的氢氧化铜悬浊液,加热,产生砖红色沉淀,证明淀粉发生了水解,产生葡萄糖;另一支加入少量碘水,碘水变蓝,证明还有未水解的淀粉存在.
③步骤a的操作是C.
A.蒸发 B.萃取 C.蒸馏 D分液.
(2)除去下列物质中的少量杂质(括号内为杂质),试填下表
| 物质 | 加入试剂 | 去杂提纯方法 |
| 蛋白质(NaCl) | ||
| 肥皂(甘油) |
A.蔗糖和麦芽糖互为同分异构体,二者均能与银氨溶液反应,并且水解产物相同.
B.盐析可提纯蛋白质并保持其生理活性.
C.天然植物油常温下一般呈液态,难溶于水,有固定的熔点、沸点.
D.两分子半胱氨酸(
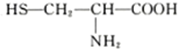 )脱水缩合形成二肽的结构简式为:
)脱水缩合形成二肽的结构简式为: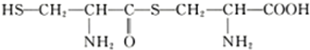 .
.(4)写出工业上由硬脂酸甘油酯制肥皂的化学方程式:
 +3NaOH $\stackrel{加热}{→}$3C17H35COONa+
+3NaOH $\stackrel{加热}{→}$3C17H35COONa+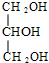 .
.
16.化学无处不在,下列与化学有关的说法正确的是( )
| A. | 氯气工厂爆炸时可用湿布捂住鼻孔、眼睛等并躲在下风的低洼处 | |
| B. | 二氧化硫可用来加工食品,使食品增白 | |
| C. | 锂可用于制造质量轻、电容量大的可充电电池 | |
| D. | 高纯度二氧化硅是制造太阳能电板的材料之一 |
6.将固体NH4I置于2L的密闭容器中,在一定温度下发生下列反应:①NH4I(S)?MH3(g)+HI(g)
②2HI(g)?H2(g)+I2(g)达到平衡时,n(H2)=1mol,n(HI)=8mol,则此温度下反应①的平衡常数为( )
②2HI(g)?H2(g)+I2(g)达到平衡时,n(H2)=1mol,n(HI)=8mol,则此温度下反应①的平衡常数为( )
| A. | 20 | B. | 16 | C. | 9 | D. | 25 |
13.下列分子中存在同分异构体的是( )
| A. | C2H4 | B. | C4H10 | C. | CH3Cl | D. | C3H8 |
10.已知:H2、CO的燃烧热分别为-285.8kJ•mol-1、-283kJ•mol-1.现有H2与CO的混合气体33.6L(标准状况),使其完全燃烧,测得反应放热425.55kJ,则原混合气体中H2与CO的物质的量之比是 ( )
| A. | 1:1 | B. | 1:3 | C. | 1:4 | D. | 2:3 |
11.A、B、C、X均为常见物质,它们之间有如图转化关系(其它产物已略去),则下列说法不正确的是( )


| A. | 若A是H2S,则C可能是SO2 | |
| B. | 若X是强碱,则B可能是两性物质 | |
| C. | 若A是非金属单质,则C与水反应的生成物一定是强酸 | |
| D. | 若X是金属单质,则B、C中X的化合价可能是B>C |
