��Ŀ����
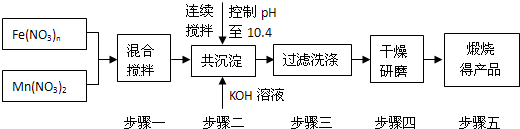
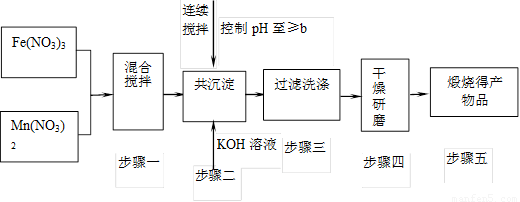
������Դ����Ľ�һ��ͻ���������Ȼ�ѧѭ��������о�Խ���ܵ�������ҵ�������������о����֣����������������̣�MnFe2O4���������Ȼ�ѧѭ���ֽ�ˮ���⣬MnFe2O4���Ʊ��������£�
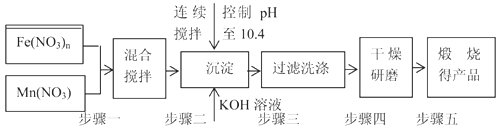
��1��ԭ��Fe��NO3��n��n��___________ ��Ͷ��ԭ��Fe��NO3��n��Mn��NO3��2�����ʵ���֮��ӦΪ_____________��
��2��������С��������衱��Ŀ����___________�� ��������ϴ�Ӹɾ��ı���___________��
��3������MnFe2O4�Ȼ�ѧѭ������ķ�Ӧ�ɱ�ʾΪ��
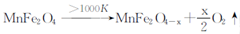 ��
��
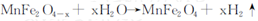
�������������������Ӧ���ش��������⣺
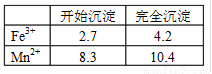
����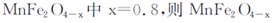 ����Fe2+ռȫ����Ԫ�صİٷ���Ϊ__________��
����Fe2+ռȫ����Ԫ�صİٷ���Ϊ__________��
�ڸû�ѧѭ��������ŵ��У������㼴�ɣ�____________ ��
�۸��Ȼ�ѧѭ�����������в���֮������һ���Ľ��ķ�����________________��
��2��������С��������衱��Ŀ����___________�� ��������ϴ�Ӹɾ��ı���___________��
��3������MnFe2O4�Ȼ�ѧѭ������ķ�Ӧ�ɱ�ʾΪ��
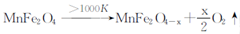 ��
��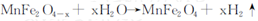
�������������������Ӧ���ش��������⣺
����
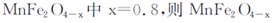 ����Fe2+ռȫ����Ԫ�صİٷ���Ϊ__________��
����Fe2+ռȫ����Ԫ�صİٷ���Ϊ__________���ڸû�ѧѭ��������ŵ��У������㼴�ɣ�____________ ��
�۸��Ȼ�ѧѭ�����������в���֮������һ���Ľ��ķ�����________________��
��1��3�� 2:1
��2����ַ�Ӧ��������ȫ��ϴ��������Һ������
��3����80% ��
�ھ��й��̼���Լ����������Ⱦ���������۲���ѭ��ʹ�ü������������ڲ�ͬ�������ɣ���˲����ڸ������������ŵ�
��Ѱ�Һ��ʵĴ�����ʹMnFe2O4�ֽ��¶Ƚ��ͻ��ҷֽ��¶ȸ��͵�������
��2����ַ�Ӧ��������ȫ��ϴ��������Һ������
��3����80% ��
�ھ��й��̼���Լ����������Ⱦ���������۲���ѭ��ʹ�ü������������ڲ�ͬ�������ɣ���˲����ڸ������������ŵ�
��Ѱ�Һ��ʵĴ�����ʹMnFe2O4�ֽ��¶Ƚ��ͻ��ҷֽ��¶ȸ��͵�������

��ϰ��ϵ�д�
�����Ŀ



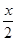 O2(g)����H1
O2(g)����H1