题目内容
分别在pH=1的酸溶液和pH=14的NaOH溶液中加入足量的铝,放出的氢气的量是前者多,其原因是( )
| A、两种溶液体积相同,而酸是多元酸 | B、.两种溶液体积相同,而酸是弱酸 | C、酸是硝酸溶液,体积和NaOH溶液相同 | D、.酸是硫酸,且酸的体积小于NaOH的体积 |
分析:在本题中,酸电离出的 C(H+)═0.1mol/L,碱液中 C(OH-)═1 mol/L,铝是足量的,所以生成氢气的量就取决于 n(H+)、n(OH-),而根据铝与酸碱的反应可知,当生成相同量的氢气时,需要的 n(H+) 都比 n(OH-)多,所以当酸生成的氢气更多时,就需要 n(H+)>n(OH-),然后结合强酸完全电离,弱酸部分电离的特点来解本题.
解答:解:由铝与酸、碱的反应可知:
2Al~6H+~3H2 2Al~2OH-~3H2
要使生成的氢气前者多,必须n(H+)>n(OH-)
A、当酸为多元强酸,由于C(H+)<C(OH-),当两种溶液体积相同时,则会有n(H+)<n(OH-),不符合题意,故A错误;
B.若酸是弱酸,虽然酸电离出的 C(H+)小于氢氧化钠中的 C(OH-),但弱酸是部分电离,此时酸中的H+ 的总量完全可以比 NaOH 中的 OH- 多 故满足n(H+)>n(OH-),符合题意,故B正确;
C.硝酸是强氧化性酸,铝与稀硝酸反应生成一氧化氮,而不是氢气,故C不符合题意,故C错误;
D.硫酸是强酸,完全电离,当酸的体积小于NaOH的体积时,n(H+)<n(OH-),不符合题意,故D错误.
故选B.
2Al~6H+~3H2 2Al~2OH-~3H2
要使生成的氢气前者多,必须n(H+)>n(OH-)
A、当酸为多元强酸,由于C(H+)<C(OH-),当两种溶液体积相同时,则会有n(H+)<n(OH-),不符合题意,故A错误;
B.若酸是弱酸,虽然酸电离出的 C(H+)小于氢氧化钠中的 C(OH-),但弱酸是部分电离,此时酸中的H+ 的总量完全可以比 NaOH 中的 OH- 多 故满足n(H+)>n(OH-),符合题意,故B正确;
C.硝酸是强氧化性酸,铝与稀硝酸反应生成一氧化氮,而不是氢气,故C不符合题意,故C错误;
D.硫酸是强酸,完全电离,当酸的体积小于NaOH的体积时,n(H+)<n(OH-),不符合题意,故D错误.
故选B.
点评:本题既考查了铝与酸碱的反应,又考查了弱电解质的电离特点,综合性较强,属于中等难度的题目.

练习册系列答案
相关题目
 甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动.实验方案如下:
甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动.实验方案如下: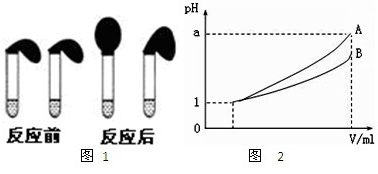

 )分别稀释至100mL,
)分别稀释至100mL,
 ,则A、B都是弱酸
,则A、B都是弱酸






 B、
B、
 D、
D、