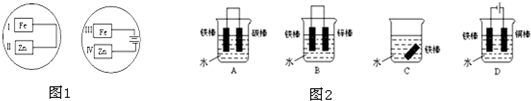
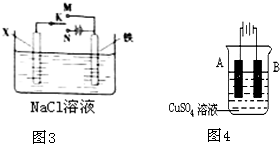
题目内容
利用反应Zn+2FeCl3====ZnCl2+2FeCl2组成一个化学电池。(1)画出装置图,并指出正极为__________,电极反应式为_______;负极为_______,电极反应式为________。
(2)若电池内溶液为100 mL 0.5 mol·L-1的FeCl3溶液;当溶液中FeCl3全部被还原成FeCl2时,溶液中ZnCl2的物质的量浓度是__________,导线上通过的电子是__________mol。
解析:自发发生的氧化反应的是Zn+2FeCl3====2FeCl2+ZnCl2,发生氧化反应的是Zn―2e-====Zn2+,发生还原反应的是2Fe3++2e-====2Fe2+,所以负极材料应为锌电极,正极材料应采用金属性比Zn弱的金属材料或非金属导电材料如石墨棒等,电解质溶液用FeCl3溶液。其装置图如图4-19所示。
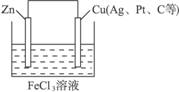
图4-19
负极为Zn,电极反应式:Zn―2e-====Zn2+;正极为Cu(或Ag、Pt、C等),电极反应式:2Fe3++2e-====2Fe2+。
(2)设n(Zn2+)=x,n(e-)=y,根据电池总反应可知
2Fe3++Zn====Zn2++2Fe2+转移电子的物质的量
2 mol 1 mol 1 mol 2 mol
0.05 mol x y
得x=0.025 mol,y=0.05 mol
c(ZnCl2)=0.025 mol/0.1 L=0.25 mol·L-1
导线上通过的电子的物质的量为0.05 mol。
答案:(1)Cu(或Ag、Pt、C等) 2Fe3++2e-====2Fe2+ Zn Zn-2e-====Zn2+
(2)0.25 mol·L-1 0.05

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(7分)二氧化锰是制造锌锰干电池的基本材料.工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下: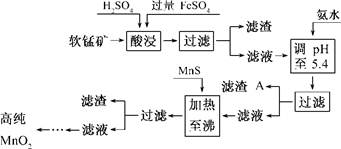
某软锰矿的主要成分为MnO2,还含Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
| 沉淀物 | pH |
| Al(OH)3 | 5.2 |
| Fe(OH)3 | 3.2 |
| Fe(OH)2 | 9.7 |
| Mn(OH)2 | 10.4 |
| Cu(OH)2 | 6.7 |
| Zn(OH)2 | 8.0 |
| CuS | ≥-0.42 |
| ZnS | ≥2.5 |
| MnS | ≥7 |
| FeS | ≥7 |
(2)滤渣A的主要成分为________.
(3)加入MnS的目的是除去________杂质.
(4)碱性锌锰干电池中,MnO2参与的电极反应方程式为__________________________.
(5)从废旧碱性锌锰干电池中可以回收利用的物质有________(写出两种).
科研人员将软锰矿(MnO2含量≥65%,SiO2含量约20%,A12O3含量约4%,其余为水分)和闪锌矿(ZnS含量≥80%,FeS、CuS、SiO2含量约7%,其余为水分)同槽酸浸开发出综合利用这两种资源的新工艺,如图所示为工艺流程的一部分.
已知:ZnCO3不溶于水,但溶于酸.部分阳离子以氢氧化物形式深沉时溶液的pH见下表:
| 物质 | Fe(OH)3 | A1(OH)3 | Zn(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 3.3 | 5.4 | 7.6 | 8.3 |
| 完全沉淀pH | 4.4 | 5.2 | 8.0 | 9.6 | 9.8 |
(1)反应器I过滤所得滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、A12(CO4)3等.试完成反应器I中生成CuSO4的化学方程式(不须配平):CuS+______+H2SO4→______+______+CuSO4+H2O
(2)反应器II中发生反应的离子方程式为______.
(3)从沉淀溶解平衡的角度分析反应器III中生成A1(OH)3沉淀的原因______.检验ZnCO3是否过量的操作方法是______.
(4)反应器中IV中,试剂A可以是下列物质中______(填代号).a.氨水 b.氢氧化钠 c.MnO2 d.稀硫酸
(5)欲从反应器IV的滤液中完全沉淀出Zn(OH)2,而不析出Mn(OH)2,则滤液的pH范围为______,要将分离出沉淀后的滤液进行浓缩,需将温度控制在90℃~100℃,可采用的加热方法是______.

已知:ZnCO3不溶于水,但溶于酸.部分阳离子以氢氧化物形式深沉时溶液的pH见下表:
| 物质 | Fe(OH)3 | A1(OH)3 | Zn(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 3.3 | 5.4 | 7.6 | 8.3 |
| 完全沉淀pH | 4.4 | 5.2 | 8.0 | 9.6 | 9.8 |
(1)反应器I过滤所得滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、A12(CO4)3等.试完成反应器I中生成CuSO4的化学方程式(不须配平):CuS+______+H2SO4→______+______+CuSO4+H2O
(2)反应器II中发生反应的离子方程式为______.
(3)从沉淀溶解平衡的角度分析反应器III中生成A1(OH)3沉淀的原因______.检验ZnCO3是否过量的操作方法是______.
(4)反应器中IV中,试剂A可以是下列物质中______(填代号).a.氨水 b.氢氧化钠 c.MnO2 d.稀硫酸
(5)欲从反应器IV的滤液中完全沉淀出Zn(OH)2,而不析出Mn(OH)2,则滤液的pH范围为______,要将分离出沉淀后的滤液进行浓缩,需将温度控制在90℃~100℃,可采用的加热方法是______.