题目内容
设NA为阿伏加德罗常数,下列叙述正确的是
- A.标准状况下,11.2LH2O所含分子数为0.5NA
- B.1 mol·L-1CaCl2溶液中所含Ca2+离子的数目为NA
- C.通常状况下,32gO2与32gO3所含的氧原子数均为2NA
- D.7.1gCl2与足量的氢氧化钠溶液反应转移的电子数为0.2NA
C
A:错在:没有明确气体摩尔体积使用的条件,和标准状况含义为:0℃ 一个标准大气压。此时水为固液混合体。
B:错在:没有明确物质的量浓度的含义。钙离子个应该要知道溶液的体积。
C:正确。正确理解摩尔质量的计算公式和抓住两种物质组成的共同点:n(O)=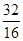 ="2" mol
="2" mol
D:错在:没有明确化学反应中作氧化剂和还原剂的氯气比为:1︰1
Cl2 + 2NaOH =" NaCl" + NaClO + H2O
n(Cl2)=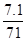 =" 0.1" mol 作氧化剂的为:0.1÷2=" 0.05" mol
=" 0.1" mol 作氧化剂的为:0.1÷2=" 0.05" mol
转移电子为:0.05×2 =" 0.1" mol 则个数为:0.1NA
A:错在:没有明确气体摩尔体积使用的条件,和标准状况含义为:0℃ 一个标准大气压。此时水为固液混合体。
B:错在:没有明确物质的量浓度的含义。钙离子个应该要知道溶液的体积。
C:正确。正确理解摩尔质量的计算公式和抓住两种物质组成的共同点:n(O)=
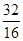 ="2" mol
="2" molD:错在:没有明确化学反应中作氧化剂和还原剂的氯气比为:1︰1
Cl2 + 2NaOH =" NaCl" + NaClO + H2O
n(Cl2)=
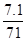 =" 0.1" mol 作氧化剂的为:0.1÷2=" 0.05" mol
=" 0.1" mol 作氧化剂的为:0.1÷2=" 0.05" mol转移电子为:0.05×2 =" 0.1" mol 则个数为:0.1NA

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
设NA为阿伏加德罗常数值,下列说法不正确的是
| A.1 mol O2与金属钠反应,O2不一定得到4NA个电子 |
| B.标准状况下,a L CH4和a L C6H14中所含分子数均为a NA/22.4 |
| C.常温常压下,1 mol氯气与足量的金属镁反应,转移2NA个电子 |
| D.在20 ℃、1.01×105 Pa时,2.8 g C2H4和CO的混合气体含气体分子数等于0.1 NA |