题目内容
17.用NA表示阿伏伽德罗常数的值,下列说法正确的是( )| A. | 1molN2所含有的原子数为NA | |
| B. | 标准状况下,16gNH3中含有的分子数为NA | |
| C. | 标准状况下,22.4L氯化氢所含的原子数为NA | |
| D. | 500ml 1.0mol•L-1硫酸钠溶液中所含的钠离子数为NA |
分析 A.氮气为双原子分子,1mol氮气中含有2mol氮原子;
B.氨气的摩尔质量为17g/mol,16g氨气的物质的量小于1mol;
C.标况下22.4L氯化氢的物质的量为1mol,1mol氯化氢中含有2mol原子;
D.根据n=cV计算出硫酸钠的物质的量,再计算出钠离子的物质的量及数目.
解答 解:A.1mol氮气中含有2mol氮原子,所含有的原子数为2NA,故A错误;
B.16g氨气的物质的量小于1mol,含有的分子数小于NA,故B错误;
C.标况下,22.4L氯化氢的物质的量为1mol,含有2mol原子,所含的原子数为2NA,故C错误;
D.500mL 1.0 mol•L-1硫酸钠溶液中含有溶质0.5mol,0.5mol硫酸钠中含有1mol钠离子,所含的钠离子数为NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确分子、原子、原子核内质子中子及核外电子的构成关系,选项B为易错点,注意氨气的摩尔质量为17g/mol.

练习册系列答案
相关题目
7.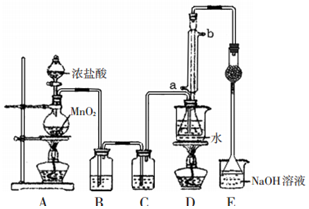 S2Cl2是工业上常用的硫化剂,实验室利用反应:CS2+3Cl2=CCl4+S2Cl2来制备S2Cl2,反应装置如图所示(部分夹持装置省略).
S2Cl2是工业上常用的硫化剂,实验室利用反应:CS2+3Cl2=CCl4+S2Cl2来制备S2Cl2,反应装置如图所示(部分夹持装置省略).
已知:S2Cl2易与水反应.
下列是几种物质的熔沸点.
(1)写出装置A中制备Cl2的化学反应方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)装置B中盛放试剂的作用是吸收Cl2中的HCl气体; 装置C中的试剂是浓硫酸.
(3)D装置中采用水浴加热的优点是受热均匀,温度易控制; 反应结束后,从D装置锥形瓶内的混合物中分离出产物S2Cl2的实验方法是蒸馏.
(4)装置E中倒扣漏斗的作用是防止倒吸.
(5)S2Cl2易与水反应,有淡黄色沉淀生成,产生的无色气体能使品红溶液褪色,写出该反应的化学方程式2S2Cl2+2H2O=3S↓+SO2↑+4HCl.
 S2Cl2是工业上常用的硫化剂,实验室利用反应:CS2+3Cl2=CCl4+S2Cl2来制备S2Cl2,反应装置如图所示(部分夹持装置省略).
S2Cl2是工业上常用的硫化剂,实验室利用反应:CS2+3Cl2=CCl4+S2Cl2来制备S2Cl2,反应装置如图所示(部分夹持装置省略).已知:S2Cl2易与水反应.
下列是几种物质的熔沸点.
| 物质 | 沸点/℃ | 熔点/℃ |
| CS2 | 47 | -109 |
| CCl4 | 77 | -23 |
| S2Cl2 | 137 | -77 |
(2)装置B中盛放试剂的作用是吸收Cl2中的HCl气体; 装置C中的试剂是浓硫酸.
(3)D装置中采用水浴加热的优点是受热均匀,温度易控制; 反应结束后,从D装置锥形瓶内的混合物中分离出产物S2Cl2的实验方法是蒸馏.
(4)装置E中倒扣漏斗的作用是防止倒吸.
(5)S2Cl2易与水反应,有淡黄色沉淀生成,产生的无色气体能使品红溶液褪色,写出该反应的化学方程式2S2Cl2+2H2O=3S↓+SO2↑+4HCl.
8.分子式为C5H12O的醇有多种结构,其中能发生催化氧化生成醛的结构有(不考虑立体异构)( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
5.下列物质在光照时不反应的是( )
| A. | 氢气和氯气的混合气体 | B. | 硝酸 | ||
| C. | 氢气和氧气的混合气体 | D. | 氯水 |
12.下列物质中同时含有氯气分子和氯离子的是( )
| A. | 液氯 | B. | 次氯酸 | C. | CaCl2溶液 | D. | 新制氯水 |
2.有机物M、N、Q之间的转化关系为 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | M的同分异构体有3种(不考虑立体异构) | |
| B. | N分子中所有原子共平面 | |
| C. | Q的名称为异丙烷 | |
| D. | M、N、Q均能与Br2反应 |
9.下列颜色变化不是因为发生化学变化而产生的是( )
| A. | 漂白粉使某些有机颜料褪色 | |
| B. | 一氧化氮气体在空气中变为红棕色 | |
| C. | 用二氧化硫漂白纸浆、毛、丝、草帽辫等 | |
| D. | 向红墨水中投入活性炭,红色褪去 |
6.下列物质使用(括号内为用途)不正确的是( )
| A. | 碳酸钠(发酵粉) | B. | Ca(ClO)2(消毒剂) | C. | Al2O3(耐火材料) | D. | 过氧化钠(供氧剂) |