题目内容
用8.70 g MnO2和125 g质量分数为36.5%的盐酸作用制取Cl2,求:
(1)最多生成Cl2的质量.
(2)把反应后溶液稀释至1.00 L后取出20.0 mL(不考虑HCl损失),在20.0 mL的溶液中加入足量AgNO3,可得AgCl沉淀的质量.
解析:
|
答案:(1)7.10 g (2)AgCl的质量为30.1 g 解析:利用Cl-的物质的量守恒:原Cl-的物质的量n=1.25 mol,生成Cl2时消耗Cl- 0.2 mol,故溶液中剩余的Cl-的物质的量为1.05 mol,取出1/5,则与AgNO3溶液反应的Cl-的物质的量为0.210 mol,则可生成AgCl 0.210 mol,合30.1 g. |

 同步轻松练习系列答案
同步轻松练习系列答案
| |||||||||||||||||||||||||||||||||||
| |||||||||||||||||||
 Mn2++Cl2↑+2H2O,也可以利用反应:
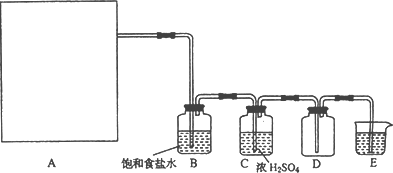
Mn2++Cl2↑+2H2O,也可以利用反应: 2KCl+2MnCl2+5Cl2↑+8H2O制取并收集纯净、干燥的氯气,部分装置如图所示:
2KCl+2MnCl2+5Cl2↑+8H2O制取并收集纯净、干燥的氯气,部分装置如图所示: