题目内容
某工厂用软锰矿(含MnO2约70%及Al2O3)和闪锌矿(含ZnS约80%及FeS)共同生产MnO2和Zn(干电池原料):已知①A是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液.②IV中的电解反应式为MnSO4+ZnSO4+2H2O
 MnO2+Zn+2H2SO4.
MnO2+Zn+2H2SO4.
(1)A中属于还原产物的是______.
(2)MnCO3、Zn2(OH)2CO3的作用是______;II需要加热的原因是______;C的化学式是______.
(3)该生产中除得到MnO2和Zn以外,还可得到的副产品是______.
(4)如果不考虑生产中的损耗,除矿石外,需购买的化工原料是______.
(5)要从Na2SO4溶液中得到芒硝,需进行的操作有蒸发浓缩、______、过滤、洗涤、干燥等.
(6)从生产MnO2和Zn的角度计算,软锰矿和闪锌矿的质量比大约是______.
【答案】分析:(1)比较信息①A与软锰矿中元素化合价的变化可知,A中还原产物为MnSO4.
(2)由工艺流程可知,A中加入MnCO3、Zn2(OH)2CO3,A中的Fe3+、Al3+,经过一系列操作转化为氧化铁、氧化铝.
Fe3+、Al3+沉淀时容易形成胶体,不利于氢氧化铁、氢氧化铝沉降.
操作Ⅰ加热、浸取需要硫酸,由②可知C为硫酸,循环利用.
(3)根据流程图不难得出副产物有硫、氧化铁、氧化铝,
(4)除矿石外,需加入的物质,就是要购买的化工原料.
(5)从溶液中获得固体物质,需蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(6)设软锰矿、闪锌矿的质量分别为x、y,根据②可知MnO2、Zn的物质的量之比为1:1,据此列放出计算x:y的值.
解答:解:(1)比较信息①A与软锰矿中元素化合价的变化可知,Mn元素化合价由+4价降低为+2价,所以A中还原产物为MnSO4.
故答案为:MnSO4.
(2)由工艺流程可知,MnCO3、Zn2(OH)2CO3的作用就是调节pH,使Fe3+、Al3+沉淀完全.
Fe3+、Al3+沉淀容易形成胶体,不利于氢氧化铁、氢氧化铝沉降,Ⅱ中加热的目的是加速沉淀生成,防止胶体出现,并使形成胶体的氢氧化铝和氢氧化铁也生成沉淀.
操作Ⅰ加热、浸取需要硫酸,由②可知C为硫酸,循环利用.
故答案为:调节溶液的pH,使Fe3+和 Al3+生成沉淀;加速沉淀生成,防止胶体出现,并使形成胶体的氢氧化铝和氢氧化铁也生成沉淀;H2SO4.
(3)根据流程图可知,副产物有硫、氧化铁、氧化铝.
故答案为:硫、氧化铁、氧化铝.
(4)根据流程图可知,需要加入碳酸钠、硫酸,所以除矿石外,需购买的化工原料是碳酸钠、硫酸.
故答案为:碳酸钠、硫酸.
(5)从溶液中获得固体物质,需蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
故答案为:冷却结晶.
(6)设软锰矿、闪锌矿的质量分别为xg、yg,根据②可知MnO2、Zn的物质的量之比为1:1,则:
 :
: =1:1,解得x:y=1.03.
=1:1,解得x:y=1.03.
故答案为:1.03.
点评:本实验的目的是制备二氧化锰与锌,因而需要把氧化铝、铁元素、硫元素除去.据此考查学生对工艺流程的理解、物质性质、氧化还原反应、分离提纯基本操作、化学计算等,难度中等,关键是掌握整个制备流程原理,要求学生要有扎实的基础知识和灵活应用知识解决问题的能力.
(2)由工艺流程可知,A中加入MnCO3、Zn2(OH)2CO3,A中的Fe3+、Al3+,经过一系列操作转化为氧化铁、氧化铝.
Fe3+、Al3+沉淀时容易形成胶体,不利于氢氧化铁、氢氧化铝沉降.
操作Ⅰ加热、浸取需要硫酸,由②可知C为硫酸,循环利用.
(3)根据流程图不难得出副产物有硫、氧化铁、氧化铝,
(4)除矿石外,需加入的物质,就是要购买的化工原料.
(5)从溶液中获得固体物质,需蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(6)设软锰矿、闪锌矿的质量分别为x、y,根据②可知MnO2、Zn的物质的量之比为1:1,据此列放出计算x:y的值.
解答:解:(1)比较信息①A与软锰矿中元素化合价的变化可知,Mn元素化合价由+4价降低为+2价,所以A中还原产物为MnSO4.
故答案为:MnSO4.
(2)由工艺流程可知,MnCO3、Zn2(OH)2CO3的作用就是调节pH,使Fe3+、Al3+沉淀完全.
Fe3+、Al3+沉淀容易形成胶体,不利于氢氧化铁、氢氧化铝沉降,Ⅱ中加热的目的是加速沉淀生成,防止胶体出现,并使形成胶体的氢氧化铝和氢氧化铁也生成沉淀.
操作Ⅰ加热、浸取需要硫酸,由②可知C为硫酸,循环利用.
故答案为:调节溶液的pH,使Fe3+和 Al3+生成沉淀;加速沉淀生成,防止胶体出现,并使形成胶体的氢氧化铝和氢氧化铁也生成沉淀;H2SO4.
(3)根据流程图可知,副产物有硫、氧化铁、氧化铝.
故答案为:硫、氧化铁、氧化铝.
(4)根据流程图可知,需要加入碳酸钠、硫酸,所以除矿石外,需购买的化工原料是碳酸钠、硫酸.
故答案为:碳酸钠、硫酸.
(5)从溶液中获得固体物质,需蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
故答案为:冷却结晶.
(6)设软锰矿、闪锌矿的质量分别为xg、yg,根据②可知MnO2、Zn的物质的量之比为1:1,则:
 :
: =1:1,解得x:y=1.03.
=1:1,解得x:y=1.03.故答案为:1.03.
点评:本实验的目的是制备二氧化锰与锌,因而需要把氧化铝、铁元素、硫元素除去.据此考查学生对工艺流程的理解、物质性质、氧化还原反应、分离提纯基本操作、化学计算等,难度中等,关键是掌握整个制备流程原理,要求学生要有扎实的基础知识和灵活应用知识解决问题的能力.

练习册系列答案
相关题目
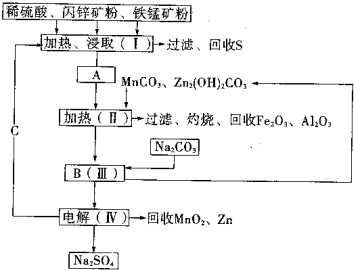 (2011?湖南模拟)某工厂用软锰矿(含MnO2约70%及少量Al2O3)和闪锌矿(古ZnS约80%及少量FeS)共同生产MnO2和Zn(干电池原料)生产工艺如下:
(2011?湖南模拟)某工厂用软锰矿(含MnO2约70%及少量Al2O3)和闪锌矿(古ZnS约80%及少量FeS)共同生产MnO2和Zn(干电池原料)生产工艺如下: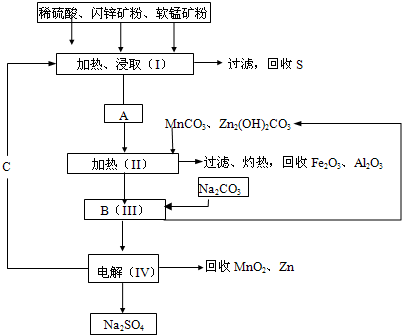
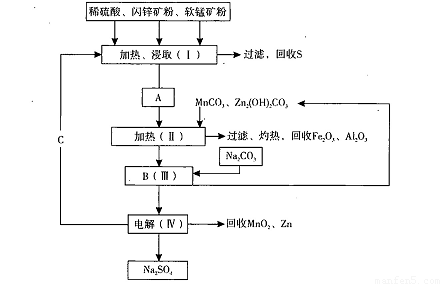
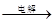 MnO2+Zn +2H2SO4。
MnO2+Zn +2H2SO4。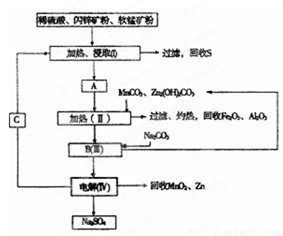
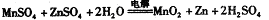
 MnO2+Zn+2H2SO4。
MnO2+Zn+2H2SO4。